已知2H2(g)+O2(g) →2H2O(l)+571.6kJ,2H2(g)+O2(g) →2H2O(g)+483.6kJ。下列说法正确的是
| A.2 molH2(g)和1molO2(g)的总能量小于2mol H2O (l)的能量 |
| B.1 mol H2O (g)分解成H2(g)和O2 (g),吸收241.8kJ能量 |
| C.1mol H2O (l)变成1mo1 H2O (g),吸收88 kJ能量 |
| D.等质量的H2O (g)比H2O(l)所含能量低 |
已知33As、35Br位于同一周期,下列关系正确的是
| A.原子半径:As>C1>P | B.热稳定性:HC1>AsH3>HBr |
| C.还原性:As3->S2->C1- | D.酸性:H3AsO4>H2SO4>H3PO4 |
下列各组离子能大量共存于同一溶液中,且加入过量NaOH溶液或少量稀H2SO4时,都能产生白色沉淀的是
| A.Ba2+、Mg2+、NO3-、CO32- | B.Na+、Al3+、Cl-、AlO2- |
| C.Ba2+、K+、Cl-、HCO3- | D.NH4+、Fe3+、Ba2+、Cl- |
香柠檬酚具有抗氧化功能,它的结构简式如右图,下列说法正确的是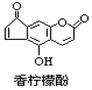
| A.它的分子式为C13H9O4 |
| B.它与H2发生加成反应,1mol最多可消耗7mol H2 |
| C.它与Br2发生取代反应,1mol最多消耗3mol Br2 |
| D.它与NaOH溶液反应,1mol最多消耗3molNaOH |
钛被誉为“21世纪金属”。工业冶炼钛的第一步反应为:
TiO2+2C+2Cl2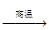 TiCl4+2CO。下列关于该反应的说法正确的是
TiCl4+2CO。下列关于该反应的说法正确的是
| A.TiO2是氧化剂 |
| B.氧化剂与还原剂的物质的量之比为1:1 |
| C.Cl2发生氧化反应 |
| D.当2 mol C参加反应时,转移的电子数目为2 mol |