X元素的阳离子和Y元素的阴离子具有相同的电子层结构,下列叙述正确的是( )
| A.原子序数:X<Y | B.原子半径:X<Y | C.离子半径:X>Y | D.电负性:X<Y |
短周期元素甲、乙、丙、丁的原子半径依次增大,其氢化物中甲、乙、丙、丁的化合价如右表所示。下列说法中正确的是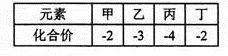
| A.元素非金属性:甲<乙 |
| B.含氧酸的酸性:乙<丁 |
| C.氢化物的沸点:甲>丁 |
| D.丙所形成的单质可能互为同位素 |
反应中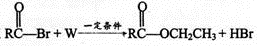 ,W为
,W为
| A.CH3CHO | B.CH3CH2OH |
| C.CH3COOH | D.H2O |
下列说法错误的是
| A.金属钠着火可用干燥沙土扑灭 |
| B.地沟油经处理后可用作生物柴油 |
| C.糖类、油脂、蛋白质均为高分子化合物 |
| D.氢氧化铁胶体的分散质粒子能通过滤纸孔隙 |
已知某溶液中含有下列8种离子中的5种(忽略水的电离及离子的水解):K+、Cu2+、Al3+、Fe2+、Cl-、CO32-、NO3-、SO42-,且5种离子的物质的量浓度相等。为了进一步探究该水溶液的组成,某同学进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰。
②另取溶液加入足量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
③另取溶液加入BaCl2溶液,有白色沉淀生成。
根据上述实验,以下推测正确的是
| A.无法确定溶液中是否存在Cu2+离子 |
| B.原溶液中不含K+、Al3+、CO32-等离子 |
| C.根据步骤②只能确定溶液中一定存在NO3-离子 |
| D.步骤③所得到的白色沉淀共有2种钡盐 |
取未知浓度的硫酸、盐酸和醋酸各25.00mL,分別用0.10mol·L-1的NaOH溶液或0.10mol·L-1的稀氨水滴定得下图。下列说法正确的是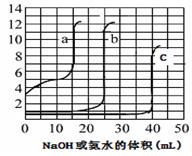
| A.由图可知曲线c为NaOH滴定硫酸 |
| B.由图可知硫酸的物质的量浓度大于盐酸的物质的量浓度 |
| C.曲线b、c的滴定实验可用酚酞做指示剂 |
| D.由图可知滴定前醋酸电离度约为1.67﹪ |