下列化学用语书写正确的是 ( )
A.氯原子的结构示意图: |
B.作为相对原子质量测定标准的碳核素: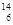 C C |
C.氯化镁的电子式: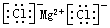 |
D.用电子式表示氯化氢分子的形成过程: |
对于反应:C(S)+H2O(g)=CO(g)+H2(g),△H>0,为了提高C(S)的转化率,可采取的措施是
| A.多加入C(S) | B.升高反应温度 | C.增大压强 | D.使用催化剂 |
已知25℃、101kPa条件下:
4Al ( s) + 3O2 (g) =2Al2O3 (s) ,△H =" -2834.9" kJ·mol-1;
s) + 3O2 (g) =2Al2O3 (s) ,△H =" -2834.9" kJ·mol-1;
4Al (s) +2O3 (g) =2Al2O3 (s) ,△H =" -3119.91" kJ·mol-1.
由此得出的结论正确的是
| A.3O2(g)=2O3(g),△H =285.01kJ·mol-1; |
| B.3O2(g)=2O3(g),△H =" -285.01" kJ·mol-1; |
| C.2O3(g)=3O2(g),△H =" +285.01" kJ·mol-1; |
| D.2O3(g)=3O2(g),△H =" -285.01" kJ·mol-1. |
有机物的天然提取和人工合成往往得到的是混合物,假设给你一种这样的有机混合物让你研究,一般要采取的几个步骤是
| A.分离、提纯→确定化学式→确定实验式→确定结构式 |
| B.分离、提纯→确定实验式→确定化学式→确定结构式 |
| C.分离、提纯→确定结构式→确定实验式→确定化学式 |
| D.确定化学式→确定实验式→确定结构式→分离、提纯 |
根据下列反应步骤,由2-丙醇转化为1,2—丙二醇(HOCH2—CHOH—CH3)的正确的反应类型的顺序是
| A.消去―加成―水解 | B.取代―消去―加成 |
| C.消去―取代―加成 | D.水解―取代―取代 |
巴豆酸的结构简式为CH3-CH=CH-COOH,现有
①溴水②氢氧化钠溶液③2-丙醇④酸化的高锰酸钾溶液。
试根据其结构特点判断在一定条件下能与巴豆酸反应的物质组合是
| A.①④ | B.①③④ |
C.②③ | D.①②③④ |