短周期元素离子aA2+、bB+、cC3-、dD-具有相同电子层结构,下列叙述正确的是( )
| A.原子半径A >B>C> D | B.原子序数 A >B>D> C |
| C.离子半径C>D>B>A | D.单质的还原性A>B>D>C |
今有如下三个热化学方程式:
H2(g)+1/2O2(g)=H2O(g);ΔH=aKJ·mol-1,
H2(g)+1/2O2(g)=H2O(l);ΔH==bkJ·mol-1,
2H2(g)+O2(g)=2H2O(l);ΔH==ckJ·mol-1,
关于它们的下列表述正确的是
| A.它们都是吸热反应 | B.a.b和c均为正值 |
| C.a==b | D.2b==c |
下图是关于反应A2(g)+3B2(g)===2C(g)△H<0的平衡移动图形,影响平衡移动的原因是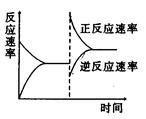
| A.升高温度,同时加压。 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时使用催化剂; |
| D.增大反应物浓度,同时减小生成物浓度 |
反应A+3B===2C+2D在四种不同情况下的反应速率分别为:
①v(A)=0.15mol/(L·s) ②v(B)=0.6 mol/(L·s) ③v(C)=0.4 mol/(L·s)④v(D)=0.45 mol/(L·s)其中,反应进行得最快的是
A.① B.② C.③ D.④
某温度下,浓度都是1mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z,经过t min后,测得物质的浓度分别为c(X2)=0.4 mol/L,c(Y2)=0.8 mol/L,c(Z)=0.4 mol/L,则该反应的反应式可以表示为
| A.X2+2Y2===2XY2 | B.2X2+Y2===2X2Y | C.3X2+Y2===2X3Y | D.X2+3Y2===2XY3 |
反应 2A(g) + B(g) 2C(g);△H > 0 。下列反应有利于生成C的是:
2C(g);△H > 0 。下列反应有利于生成C的是:
| A.低温、低压 | B.低温、高压 | C.高温、高压 | D.高温、低压 |