短周期元素R的原子核外电子数等于核内中子数,该元素单质7.8g与氧气充分反应可生成13g化合物RO,则该元素的价电子层是
| A.1S2 | B.2S2 | C.3S2 | D.4S2 |
下列叙述中,正确的是:
| A.钢铁腐蚀的负极反应为:Fe-3e- = Fe3+ |
| B.Mg—Al及NaOH溶液构成的原电池中负极材料为Mg |
| C.甲烷燃料电池的正极反应为:O2+2H2O+4e-=4OH- |
| D.乙醇燃料电池的电解质常用KOH,该电池的负极反应为: |
C2H5OH-12e-=2CO2↑+3H2O
有甲、乙两种溶液,甲溶液的pH是乙溶液pH的2倍,则甲溶液中c(H+)与乙溶液中c(H+)的关系是:
A.2∶1 |
B. 100∶1 | C.1∶100 | D.无法确定 |
下列说法不正确的是:
| A.乙醇、乙烯都可被酸性高锰酸钾溶液氧化 |
| B.乙烯、苯都可与溴水发生加成反应 |
| C.乙醇、乙酸都可以发生酯化反应 |
| D.淀粉、油脂都可以发生水解反应 |
下列各组离子中,在碱性溶液中共存,且加入盐酸过程中会产生气体和沉淀的是:
A.Na+ NO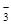 AlO AlO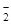 SO SO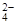 |
B.Na+ NO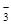 SiO SiO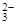 K+ K+ |
C.Na+ Cl- HCO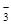 Ca2+ Ca2+ |
D.K+ Cl- AlO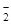 CO CO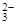 |
下列叙述正确的是:
| A.同周期元素中,ⅦA族元素的原子半径最大 |
| B.VIA族元素的原子,其半径越大,越容易得到电子 |
| C.室温时,零族元素的单质都是气体 |
| D.所有主族元素的原子,形成单原子离子时的化合价和它的族序数相等 |