将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均减小 |
| D.产生气泡的速度甲比乙快 |
下列过程一定发生化学变化的是]
| A.焰色反应检验钾元素 | B.石油的分馏 |
| C.氯水久置颜色变浅 | D.用四氯化碳萃取碘水中的碘 |
以节能减排为基础的低碳经济是保持社会可持续发展的战略举措。下列做法符合低碳经济的是
| A.大力推广塑料制品的使用 |
| B.大力发展公共交通,适度控制私家车规模 |
| C.提倡使用一次性生活用品,方便人们生活 |
| D.大量进口石油,满足国内经济发展需求 |
一定量的某有机物完全燃烧后,将燃烧产物通过足量的石灰水,经过滤可得沉淀10g,但称量滤液时,其质量只比原石灰水减少2.9g,则此有机物可能是
| A.乙醇 | B.乙二醇 | C.乙烯 | D.乙醚 |
下图表示在催化剂作用下将X和Y合成具有生物活性的物质Z,W是中间产物(R1、R2均为烃基)。
则下列有关叙述不正确的是
| A.反应①属于加成反应 | B.1molW完全加成需要4molH2 |
| C.X核磁共振氢谱有四个峰 | D.X、Y、W、Z都能与NaOH溶液反应 |
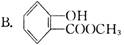
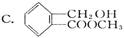
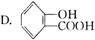
一定量的某有机物溶解于适量的NaOH溶液中,滴入酚酞试液呈现红色,煮沸5 min后溶液颜色变浅,再加入盐酸至酸性时,沉淀出白色晶体。取少量晶体放在FeCl3溶液中,溶液呈现紫色。该有机物可能是