能正确表示下列反应的离子方程式为
| A.澄清石灰水与过量NaHCO3溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| B.硫酸氢钠溶液与氢氧化钡溶液混合: SO42- + Ba2+ = BaSO4↓ |
| C.向AlCl3溶液中加入过量的氨水: Al3++ 4NH3·H2O=AlO2- + 4NH4+ + 2 H2O |
D.大理石溶于醋酸中:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2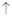 +H2O +H2O |
对于放热反应 2H2(g)+O2(g)= 2H2O(l),下列说法正确的是
| A.产物H2O所具有的总能量高于反应物H2和O2所具有的总能量 |
| B.反应物H2和O2所具有的总能量高于产物H2O所具有的总能量 |
| C.反应物H2和O2所具有的总能量等于产物H2O所具有的总能量 |
| D.反应物H2和O2比产物H2O稳定 |
Cl2、HCl的混合气体通入足量的NaOH溶液,充分反应后,溶液中除大量OH-外,还有Cl-、ClO-、 ClO3- ,且这三种离子的物质的量之比为9:2:1,则原混合气体中Cl2和HCl体积之比为
| A.5:2 | B.2:5 | C.3:1 | D.1:3 |
用NA表示阿伏加德罗常数的值,下列判断正确的是
| A.2 g H2含有的氢原子数目为NA |
| B.常温下,1 mol Cl2与足量NaOH溶液完全反应,转移的电子数为2NA |
| C.常温常压下,11.2 L氧气含有的原子数目为NA |
| D.1 L 1 mol·L-1 KOH溶液中含有的钾离子数目为NA |
下列反应的离子方程式书写正确的是
| A.盐酸与氨水的反应:H++OH-===H2O |
| B.铝与NaOH溶液的反应:Al+2OH-===AlO+H2↑ |
| C.氯气与氯化亚铁溶液的反应:Cl2+2Fe2+="==" 2Cl-+ 2Fe3+ |
| D.铜与稀硝酸的反应:Cu+2H++NO===Cu2++NO2↑+H2O |
下列电离方程式错误的是
| A.CaCl2 =Ca2++2Cl- | B.NaHCO3=Na++H++CO32- |
| C.HNO3=H++NO3- | D.Ba(OH)2=Ba2++2OH- |