验证淀粉水解可生成葡萄糖,进行了下列实验,该实验中操作步骤的排列顺序正确的是①取少量淀粉加水制成溶液 ②加热煮沸 ③加入Cu(OH)2悬浊液 ④加入几滴稀硫酸 ⑤再加热 ⑥加入NaOH溶液,调PH至碱性 ( )
| A.①②④⑤③⑥ | B.①④②③⑥⑤ |
| C.①⑤②⑥④③ | D.①④②⑥③⑤ |
以溴乙烷为原料,用下述六种反应的类型:(1)氧化(2)消去(3)加成(4)酯化
(5)水解(6)加聚,来合成乙二酸乙二酯的正确顺序()
| A.(1)(5)(2)(3)(4) | B.(1)(2)(3)(4)(5) |
| C.(2)(3)(5)(1)(4) | D.(2)(3)(5)(1)(6) |
将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I (s)  NH3(g)+HI(g);②2HI(g)
NH3(g)+HI(g);②2HI(g) H2(g)+I2(g)达到平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则此温度下反应①的平衡常数为
H2(g)+I2(g)达到平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则此温度下反应①的平衡常数为
| A.9 | B.16 | C.20 | D.25 |
下列关于可逆反应:2SO2 + O2 2SO3的说法正确的是
2SO3的说法正确的是
| A.1mol SO2与足量O2反应,可以生成1mol SO3 |
| B.平衡时,c(SO2)∶c(O2) ∶c(SO3)=2∶1∶2 |
| C.当O2的质量不再变化时,反应达到平衡 |
| D.当反应达到平衡状态时,v(O2)=0 |
下列各表述与示意图一致的是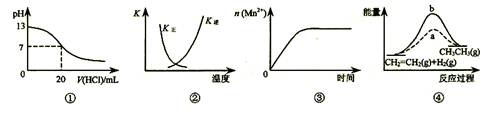
| A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
B.图②中曲线表示反应2SO2(g) + O2(g)  2SO3(g) ΔH < 0 ,正、逆反应的平衡常数K随温度的变化 2SO3(g) ΔH < 0 ,正、逆反应的平衡常数K随温度的变化 |
|
C.图③表示10 mL 0.01 mol·L-1KMnO4酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化(已知Mn2+是KMnO4酸性溶液与H2C2O4反应的催化剂 ) |
D.图④中a、b曲线分别表示反应CH2=CH2 (g) + H2(g) CH3CH3(g) ΔH< 0使用和未使用催化剂时,反应过程中的能量变化 |