下图是元素周期表的框架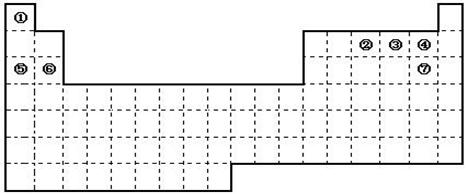
(1)请在上面元素周期表中画出金属元素与非金属元素的分界线。
(2)依据元素周期表回答下列问题:
| A.周期表中的元素⑤和元素⑥的最高价氧化物的水化物碱性强弱顺序是(用化学式表示)。 |
| B.周期表中的元素④和元素⑦的氢化物的熔、沸点高低顺序是(用化学式表示)。 |
| C.①~⑦元素的单质,在常温下化学性质稳定,通常可用作保护气的是(填写结构式)。 |
| D.在上面元素周期表中全部是金属元素的主族是;全部是非金属元素的主族是(填写字母a、b、c、d)。 |
a.ⅠA族 b. ⅡA族 c. ⅥA 族 d.ⅦA族
(3)已知甲元素位于第三周期,且其原子半径为同周期金属元素中原子半径最小的,请写出甲的氧化物与NaOH溶液反应的离子方程式 ;
(4)请写出仅用①②④三种元素形成离子化合物的电子式_________。若用球棍模型表示①和③形成的化合物的分子结构,应该是 。
⑸ 在120℃下1g①的单质在足量③的单质中完全燃烧,放出的热量为a kJ;请写出此条件下①的单质燃烧的热化学方程式 ;
①、③两种元素的单质已被应用于字宙飞船的燃料电池中,如图所示,两个电极均由多孔性碳构成,通入的两种单质由孔隙逸出并在电极表面放电。
请回答:b是电池的 极;a电极上的电极反应式是 。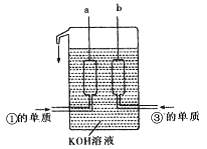
在 K2Cr2O7 + HCl —— KCl + CrCl3 + Cl2↑+ H2O反应中。
(1)氧化剂是,元素被氧化,氧化产物是。
(2)在参加反应的盐 酸中,被氧化的HCl与未被氧化的HCl的质量比为.
酸中,被氧化的HCl与未被氧化的HCl的质量比为.
(3)如果反应生成0.1molCl2,则转移电子的数目为:
有一瓶溶液只含Cl-、CO32—、SO42—、Na+、NH4+、K+、Mg2+七种离子中的某几种。经实验:
①原溶液 白色沉淀;
白色沉淀; ②将①所得溶液
②将①所得溶液 放出使湿润的红色石蕊试纸变蓝的气体;
放出使湿润的红色石蕊试纸变蓝的气体; ③原溶液
③原溶液 中加BaCl2溶液不产生沉淀。
中加BaCl2溶液不产生沉淀。 ④原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
④原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。 回答下列问题:
回答下列问题: (1) 试分析原溶液中一定含有的离子是,一定不含
(1) 试分析原溶液中一定含有的离子是,一定不含 有的离子是,可能含有的离子是。
有的离子是,可能含有的离子是。 (2) 有同学认为实验④可以省略,你认为呢?(填“可以”或“不可以”),
(2) 有同学认为实验④可以省略,你认为呢?(填“可以”或“不可以”), 并说明理由。
并说明理由。
(
有以下几种物质
| A.氯化钠 | B.硫酸(H2SO4) | C.醋酸(CH3COOH) | D.氯化银 E、酒精 F、蔗糖 |
G、氨气 H、二氧化硫 I、铜 J、硫酸钡 K、硝酸钠溶液 L、氢氧化铜
M、食盐水 N、石墨
请填空回答(填序号)。
(1)以上物质中能导电的是;
(2)以上物质中属于电解质的是;
(3)以上物质中属于非电解质的是;
(4)以上物质中既不属于电解质又不属于非电解质的是.
(每空2分共8分)
向体积不变的密闭容器中充入2 mol N2和6 mol H2,一定条件下发生反应:
N2(g)+ 3 H2(g) 2 NH3(g),平衡时混合气体共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
2 NH3(g),平衡时混合气体共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
①.若a=0,b=0,则c=
②.若a=0.7,b=2.1,则:
Ⅰ.c=.
Ⅱ.这时反应向进行.
Ⅲ.若要维持反应开始向该反应方向进行,c的范围是
(每空2分共10分)
现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为_________热反应,且m+n_________p(填“>”“=”“<”)。
(2)若增大压强,A的质量分数_________。(填“增大”“减小”或“不变”,下同)
(3)若加入B(体积不变),则B的转化率_________。
(4) 若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色_______。