在25℃101 kPa下,白磷(化学式为P4)、红磷(化学式为P)燃烧的热化学方程式分别为
P4(s)+5O2(g)= P4O10(s);△H = -3093.2 kJ/mol
4P(s)+5O2(g)= P4O10(s);△H = -2954.0 kJ/mol
由此判断,下列说法正确的是
| A.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷高 |
| B.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷低 |
| C.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷高 |
| D.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷低 |
25℃时,在浓度均为1 mol/L 的NH4Cl、NH4HCO3、NH4HSO4溶液中,测得其中c(NH4+)分别为 a、b、c(mol/L),则下列判断正确的是
| A.a>b>c | B.c>a>b | C.b>a>c | D.a>c>b |
在相同温度下,在水中分别加入下列物质,若用Kw表示水的离子积,a表示水的电离度(已电离的水分子与全部水分子的物质的量之比),则能使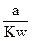 值增大的是
值增大的是
| A.Na2CO3 | B.NaHSO4 | C.NaOH | D.NaCl |
将0.02 mol/L的HCN溶液与0.02 mol/ L的NaCN溶液等体积混合,测得混合溶液中的
c (CN – ) < c (Na +),则下列关系中不正确的是
| A.c (Na+) >c (CN –) >c (OH –) >c (H+) |
| B.c (HCN) + c (CN –) =" 0.02" mol/ L |
| C.c (CN – ) > c (HCN) |
| D.c (Na+) + c (H+) =" c" (CN – ) + c (OH – ) |
pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000mL,其pH值与溶液体积的关系如图,下列说法正确的是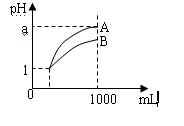
A、A、B两种酸溶液的物质的量浓度一定相等
B、稀释后,A酸溶液的酸性比B酸溶液强;
C、若a = 4,则B是强酸,A是弱酸;
D、若1< a < 4,则A、B都是弱酸。
对于可逆反应:2A(g)+B(g) 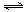 2C(g);△H<0,下列各图中正确的是
2C(g);△H<0,下列各图中正确的是