已知镁和稀硝酸反应时,每有1mol HNO3反应,就有0.8mol电子转移,此时硝酸的还原产物可能是
| A.NO2 | B.N2O | C.N2O4 | D.NO |
现有一定量的Cu和CuO混合物,向其中加入0.6 L 2.0 mol/L稀硝酸,混合物完全溶解,同时生成4.48 L NO(标准状况)。向所得溶液中加入一定体积1.0 mol/L NaOH溶液,恰好使Cu2+沉淀完全,沉淀经洗涤、充分灼烧后得32.0 g固体。(忽略溶液的体积变化)。下列说法正确的是
| A.该混合物中铜的质量为19.2 g |
| B.与该混合物反应消耗的HNO3的量为1.2 mol |
| C.加入NaOH溶液的体积是800 mL |
| D.Cu2+沉淀完全后,溶液中c(NO3-)为0.7 mol/L |
下列关于乙醇和乙酸的说法正确的是
| A.都是常用调味品的主要成分 | B.都能使紫色石蕊溶液褪色 |
| C.都能和CaCO3反应 | D.都能发生酯化反应 |
一定温度下,将2 mol SO2和1 mol O2 充入一定容密闭容器中,在催化剂存在下进行下列反应: 2SO2(g)+O2(g) 2SO3(g) △H = -197 kJ/ mol,当达到平衡状态时,下列说法中正确的是
2SO3(g) △H = -197 kJ/ mol,当达到平衡状态时,下列说法中正确的是
| A.反应放出197 kJ 的热量 | B.生成SO3为2 mol |
| C.SO2和SO3 物质的量之和为2 mol | D.SO2的物质的量和SO3 物质的量一定相等 |
下列指定反应的离子方程式正确的是
| A.向铁粉中加入足量稀硝酸:2Fe+6H+=2Fe3++3H2↑ |
| B.NO2溶于水:3NO2+H2O= 2H++2NO3–+NO |
| C.氢氧化铜与稀硝酸反应:H++OH– = H2O |
| D.向AlCl3溶液中滴加浓氨水至过量:Al3++4OH-=AlO2-+2H2O |
X、Y、Z、W为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是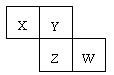
| A.原子半径:W >Z >X |
| B.非金属性:Z>Y |
| C.最高化合价:Z >X |
| D.最高价氧化物对应水化物的酸性:W>Z |