已知A物质的分子结构简式如图所示, l mol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为( )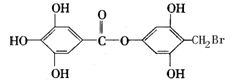
| A.6mol | B.7mol | C.8mo1 | D.9mo1 |
下列“油”中都属于油脂的是( )
①豆油 ②酱油 ③牛油 ④甘油 ⑤汽油
| A.①③ | B.②④ |
| C.①⑤ | D.④⑤ |
在一熟苹果切片上分别滴加1滴碘水和银氨溶液,颜色变化如图所示,下列推断正确的是( )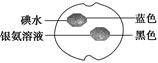
| A.熟透的苹果中含有脂肪 |
| B.熟透的苹果中不含淀粉 |
| C.熟透的苹果中含有还原性的糖 |
| D.熟透的苹果中不含还原性的糖 |
蔗糖是常见的二糖,广泛存在于甘蔗和甜菜中。下列对于蔗糖的说法中,不正确的是( )
| A.它的相对分子质量是葡萄糖的2倍 |
| B.向纯净的蔗糖溶液中加入银氨溶液,微热,不发生银镜反应 |
| C.在蔗糖与稀硫酸共热后的溶液中滴加银氨溶液,再水浴加热,看不到有银镜生成 |
| D.在蔗糖里加入浓硫酸,可观察到颜色变黑,并有泡沫出现 |
有关糖类物质概念的叙述中,正确的是( )
| A.糖类是具有甜味的物质 |
| B.糖类是具有Cn(H2O)m通式的物质 |
| C.葡萄糖是一种单糖 |
| D.淀粉是一种白色粉末,本身没有甜味,不是糖 |
从毒韭菜到炸鸡翅、从速溶茶到儿童奶粉,关于食品质量的报道中不断有①“致癌农药”、②“苏丹红”、③“碘元素”、④“亚硝酸盐”等化学名词出现。业内人士告诉记者,化学性污染正成为危及食品安全的一大“杀手”。上述化学名词所提到的物质中,在某食品添加剂中允许含有但符合限量时不会引起中毒的是( )
| A.②③④ | B.②③ |
| C.③④ | D.只有③ |