下列关于物质性质变化的比较,不正确的是( )
| A.酸性强弱:HIO4>HBrO4>HClO4 | B.原子半径大小:Na>S>O |
| C.碱性强弱:KOH>NaOH>LiOH | D.金属性强弱:Na>Mg>Al |
设NA为阿伏加德罗常数,下列说法中正确的是
| A.标准状况下11.2L Cl2溶于1L水中,转移电子的数目为0.5NA |
| B.将标准状况下22.4L NO与11.2L O2混合后的体积约为22.4L |
| C.在反应KClO4+8HCl=KCl+4Cl2↑+4H2O中,每生成4mol Cl2转移的电子数为8NA |
| D.O2和O3的混合气体共6.4g,其中所含氧原子数一定为0.4NA |
柳州的龙江河铬污染事故再一次令人触目惊心,环境保护刻不容缓。下列关于铬的一种原子Cr说法正确的是
A.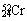 与 与 互为同素异形体 互为同素异形体 |
B.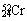 含有24个中子 含有24个中子 |
C.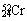 与 与 互为同位素,物理性质、化学性质均相同 互为同位素,物理性质、化学性质均相同 |
D.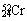 中子数比电子数多4个 中子数比电子数多4个 |
一定能在下列溶液中大量共存的离子组是
①含有大量Al3+的溶液中:Na+、NH4+、SO42—、Cl-
②加入Al能放出H2的溶液中:Cl-、HCO3—、SO42—、NH4+
③含有大量Fe3+的溶液中:Na+、Mg2+、NO3—、SCN-
④在含有大量AlO2—的溶液中:NH4+、Na+、Cl-、H+
⑤由水电离出的c(H+)=1×10-14mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3—
| A.①② | B.①③⑤ | C.① | D.①④⑤ |
下列相关反应的离子方程式书写正确的是
| A.氢氧化铁溶于氢碘酸:Fe(OH)3 +3H+ =Fe3++3H2O |
| B.向含有0.4mol FeBr2的溶液中通入0.1mol Cl2反应:2Fe2++Cl2=2Fe3+ +2Cl- |
| C.NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| D.NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3—+Ba2++2OH— = BaCO3â +2H2O+CO32— |
下列有关金属腐蚀与防护的说法正确的是
| A.银器表面在空气中因电化腐蚀渐渐变暗 |
| B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
| D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |