下列说法正确的是( )
| A.当∆H﹤0时,表示该反应为吸热反应 |
B.相同条件下,溶液中 、 、 、 、 的氧化性依次减弱 的氧化性依次减弱 |
| C.铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| D.钢铁吸氧腐蚀的正极电极反应:O2+2H2O+4e-==4OH- |
将一盛满等体积氮气和二氧化氮混合气体的试管,倒置于水槽中,片刻后水面上升的高度为试管容积的 ( )
A. |
B. |
C. |
D. |
在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示。下列说法错误的是 ( )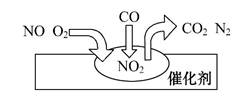
| A.NO2是该过程的中间产物 |
| B.汽车尾气的主要污染成分包括CO和NO |
| C.NO和O2必须在催化剂表面才能反应 |
D.催化转化总反应式为2NO+O2+4CO 4CO2+N2 4CO2+N2 |
某集气瓶内装的混合气体呈红棕色,加入足量蒸馏水,盖上玻璃片振荡得橙黄色溶液,气体颜色消失,再打开玻璃片后,瓶中气体又变为红棕色,该混合气体可能是 ( )
| A.N2、NO2、Br2 | B.NO2、NO、N2 |
| C.NO2、NO、O2 | D.N2、O2、Br2 |
下列关于NO2和SO2的说法错误的是 ( )
| A.NO2是一种红棕色、有毒、有刺激性气味的气体 |
| B.NO2和SO2溶于水后所得的溶液都呈酸性 |
| C.空气中的N2在闪电时,直接生成NO2 |
| D.SO2是一种无色、有刺激性气味的气体,能够漂白草帽等物质 |
某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种气体。现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是 ( )
| A.肯定有SO2和NO |
| B.肯定没有O2和NO2,可能有Cl2 |
| C.可能有Cl2和O2 |
| D.肯定只有NO |