(16分)下表为周期表的一部分,表中所列的字母分别代表一种化学元素。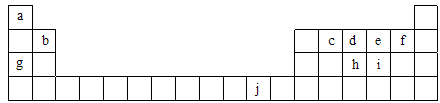
用化学用语回答下列问题:
(1)写出元素f的基态原子核外电子排布式___________________________。
(2)在c6a6分子中,元素c为 杂化,该分子是 分子(填“极性”或“非极性”)。
(3)ci2分子的电子式为_________________________,ci2与ce2比较,沸点较高的是_____________(写分子式)。
(4)第一电离能:h______i;电负性:g______b(填“>”、“<”或“=”)。
(5)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙正确是 。
| A.j位于元素周期表中第四周期、ⅠB族,属于ds区元素 |
| B.d的基态原子中,2p能级为半充满,属于p区元素 |
| C.最外层电子排布式为4s1,一定属于ⅠA族 |
| D.最外层电子排布式为ns2np1,该元素可能是ⅢA族或ⅢB族 |
(6)将氨水滴入到j的硫酸盐溶液中,先产生蓝色沉淀,然后沉淀逐渐溶解并得到深蓝色溶液,显深蓝色的离子是____________________,写出蓝色沉淀溶解在氨水中的离子方程式______________________________________________________________________。
(7)j的金属晶体的晶胞如图所示,则一个晶胞中j原子的个数是_______个。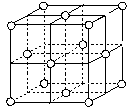
如下图,已知:①单质E可作为半导体材料;②化合物F是不成盐氧化物;③化合物I能溶于水呈酸性,它能够跟氧化物A起反应。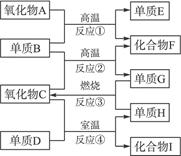
请完成下列问题:
(1)化合物F是___________________。
(2)化合物I是___________________。
(3)反应③的化学方程式是______________________________________________________。
(4)反应④的化学方程式是_____________________________________________________。
叠氮化合物应用广泛,如
,可用于汽车安全气囊,
可用于合成化合物
(见下图,仅列出部分反应条件
-代表苯基 )
)


 (1)下列说法不正确的是(填字母)
(1)下列说法不正确的是(填字母) A.反应①、④属于取代反应
A.反应①、④属于取代反应 B.化合物I可生成酯,但不能发生氧化反应
B.化合物I可生成酯,但不能发生氧化反应 C.一定条件下化合物Ⅱ能生成化合物I
C.一定条件下化合物Ⅱ能生成化合物I D.一定条件下化合物Ⅱ能与氢气反应,反应类型与反应②相同
D.一定条件下化合物Ⅱ能与氢气反应,反应类型与反应②相同 (2)化合物Ⅱ发生聚合反应的化学方程式为(不要求写出反应条件)
(2)化合物Ⅱ发生聚合反应的化学方程式为(不要求写出反应条件) (3)反应③的化学方程式为(要求写出反应条件)
(3)反应③的化学方程式为(要求写出反应条件) (4)化合物Ⅲ与
发生环加成反应成化合物
,不同条件下环加成反应还可生成化合物
的同分异构体。该同分异物的分子式为,结构式为。
(4)化合物Ⅲ与
发生环加成反应成化合物
,不同条件下环加成反应还可生成化合物
的同分异构体。该同分异物的分子式为,结构式为。 (5)科学家曾预言可合成
,其可分解成单质,用作炸药。有人通过
与
,反应成功合成了该物质下。列说法正确的是(填字母)。
(5)科学家曾预言可合成
,其可分解成单质,用作炸药。有人通过
与
,反应成功合成了该物质下。列说法正确的是(填字母)。 A.该合成反应可能是取代反应
A.该合成反应可能是取代反应 B.
与甲烷具有类似的空间结构
B.
与甲烷具有类似的空间结构 C.
不可能与化合物Ⅲ发生环加反应
C.
不可能与化合物Ⅲ发生环加反应 D.
分解爆炸的化学反应方程式可能为:
↑
D.
分解爆炸的化学反应方程式可能为:
↑
 超细氧化铝是一种重要的功能陶瓷原料。
超细氧化铝是一种重要的功能陶瓷原料。 (1)实验室常以
和
为原料,在一定条件下先反应生成沉淀
该沉淀高温分解即得超细
。
热分解的化学反应方程式。
(1)实验室常以
和
为原料,在一定条件下先反应生成沉淀
该沉淀高温分解即得超细
。
热分解的化学反应方程式。 (2)
的相对分子质量为453。欲配制100
为2、浓度约为0.1
的
溶液,配制过程为
(2)
的相对分子质量为453。欲配制100
为2、浓度约为0.1
的
溶液,配制过程为 ①用托盘天平称量
固体
;
①用托盘天平称量
固体
; ②将上述固体置于烧杯中。
②将上述固体置于烧杯中。 (3)在0.1
溶液中,铝各形态的浓度(以
计)的对数(
)随溶液
变化的关系见下图
(3)在0.1
溶液中,铝各形态的浓度(以
计)的对数(
)随溶液
变化的关系见下图

 ①用
溶液调节(2)中溶液
至7,该过程中发生反应的离子方程式有。
①用
溶液调节(2)中溶液
至7,该过程中发生反应的离子方程式有。 ②请在答题卡的框图中,画出0.01
溶液中铝各形态的浓度的对数
随溶液
变化的关系图,并进行必要的标注。
②请在答题卡的框图中,画出0.01
溶液中铝各形态的浓度的对数
随溶液
变化的关系图,并进行必要的标注。
 光催化制氢是化学研究的热点之一。科学家利用含有呲啶环(呲啶的结构式为
光催化制氢是化学研究的热点之一。科学家利用含有呲啶环(呲啶的结构式为 ,其性质类似于苯)的化合物II作为中间体,实现了循环法制氢,示意图如下(仅列出部分反应条件):
,其性质类似于苯)的化合物II作为中间体,实现了循环法制氢,示意图如下(仅列出部分反应条件):

 (1)化合物II的分子式为。
(1)化合物II的分子式为。 (2)化合物I合成方法如下(反应条件略,除化合物III的结构未标明外,反应式已配平);
(2)化合物I合成方法如下(反应条件略,除化合物III的结构未标明外,反应式已配平);

 化合物III的名称是。
化合物III的名称是。 (3)用化合物V(结构式见右图)代替III作原料,也能进行类似的上述反应,所得有机产物的结构式为。
(3)用化合物V(结构式见右图)代替III作原料,也能进行类似的上述反应,所得有机产物的结构式为。

 (4)下列说法正确的是(填字母)
(4)下列说法正确的是(填字母)
| A. | 化合物V的名称是间羟基苯甲醛,或2-羟基苯甲醛  |
B. | 化合物I具有还原性;II具有氧化性,但能被酸性高锰酸钾溶液氧化  |
C. | 化合物I、II、IV都可发生水解反应  |
D. | 化合物V遇三氯化铁显色,还可发生氧化反应,但不能发生还原反应 |
 (5)呲啶甲酸酯可作为金属离子的萃取剂。2-呲啶甲酸正丁酯(VI)的结构式见右图,其合成原料2-呲啶甲酸的结构式为;VI的同分异构体中,呲啶环上只有一个氢原子被取代的呲啶甲酸酯类同分异构体有种。
(5)呲啶甲酸酯可作为金属离子的萃取剂。2-呲啶甲酸正丁酯(VI)的结构式见右图,其合成原料2-呲啶甲酸的结构式为;VI的同分异构体中,呲啶环上只有一个氢原子被取代的呲啶甲酸酯类同分异构体有种。
已知X为FeO和CuO的混合物,取两份等质量的X样品进行下列实验: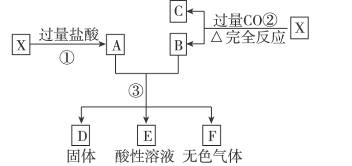
(1)写出①、②和③步所有反应的化学方程式。
(2)设第③步所得固体D的质量为32 g,溶液E中只含有一种金属离子,气体F在标准状况下体积为5.6 L,试计算取用的每份X的质量和X中FeO与CuO的质量比。