.下列说法正确的是
A.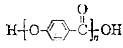 的结构中含有酯基 的结构中含有酯基 |
| B.顺-2-丁烯和反-2-丁烯的加氢产物不同 |
C.1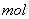 葡萄糖可水解生成2 葡萄糖可水解生成2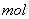 乳酸( 乳酸(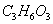 ) ) |
| D.油脂和蛋白质都是能发生水解反应的高分子化合物 |
一定温度下的难溶电解质在水溶液中达到溶解平衡时。已知下表数据
| 物质 |
Fe(OH)2 |
Cu(OH)2 |
Fe(OH)3 |
| Ksp/25℃ |
8.0×10-16 |
2.2×10-20 |
4.0×10-38 |
| 完全沉淀时的PH值 |
≥9.6 |
≥6.4 |
3~4 |
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不科学的是
A.向该溶液中加少量铁粉不能观察到红色固体析出
B.该溶液中c(SO42-):[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5:4
C.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
D.向该溶液中加入适量氯水,并调节pH值到3~4后过滤,得到纯净的CuSO4溶液
归纳法是高中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结:(均在常温下)
①pH =1的强酸溶液,加水稀释后,溶液中所有离子的浓度均降低。
②pH=2的盐酸和pH=1的醋酸,c(H+)之比为2∶1。
③在Na2CO3和NaHCO3溶液中均存在下列关系c(Na+)+c(H+)=c(OH-)+c(HCO3‑)+2c(CO32-)
④反应2A (s) + B (g)=2C (g) + D (g) 不能自发进行,则该反应△H一定大于0
⑤已知醋酸电离平衡常数为Ka;醋酸根水解常数为Kh;水的离子积为Kw;
则三者关系为:Ka·Kh=Kw
⑥反应A(g) 2B(g);△H,若正反应的活化能为EakJ·mol-1,逆反应的活化能
2B(g);△H,若正反应的活化能为EakJ·mol-1,逆反应的活化能
为EbkJ·mol-1,则△H =(Ea-Eb)kJ·mol-1。其归纳正确的是
| A.①②③⑥ | B.③④⑤⑥ | C.②④⑤⑥ | D.①③④⑤ |
下列叙述正确的是
| A.同种元素的原子均具有相同的质子数和中子数 |
| B.不同元素的原子构成的分子只含极性键 |
| C.第三周期中的非金属元素的气态氢化物还原越强,对应元素的最高价含氧酸酸性越弱 |
| D.第ⅦA族元素从上到下单质及对应的气态氢化物的沸点均逐渐升高。 |
下列各组离子在指定溶液中,能大量共存的是
①中性溶液中:Fe3+,Al3+,NO3-,I-,Cl-
②pH=11的溶液中:CO32-,Na+,AlO2-,NO3-,SO32-
③由水电离的c(H+)=10-12mol·L-1的溶液中:Cl-,K+,NO3-,NH4+,S2O32-
④加入甲基橙指示剂后显红色的溶液中:Mg2+,NH4+,Cl-,K+,SO42-
| A.①② | B.①③ | C.②④ | D.③④ |
下列说法中,正确的是
| A.铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜的熔点高于铝 |
| B.向氢氧化铁胶体中加入少量稀硫酸,因发生化学反应而产生红褐色沉淀 |
| C.电子工业用30%的氯化铁溶液腐蚀敷在印刷线路板上的铜箔:Fe3++Cu= Fe2++Cu2+ |
| D.标况下,NA个SO2分子和NA个SO3分子的体积相同(NA表示阿伏加德罗常数值) |