控制适合的条件,将反应2Fe3++2I- I2+2 Fe2+设计成如图所示的原电池。下列判断不正确的是
I2+2 Fe2+设计成如图所示的原电池。下列判断不正确的是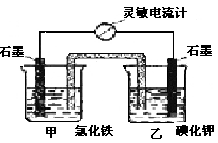
 A 反应从正向开始时,乙中石墨电极上发生氧化反应
A 反应从正向开始时,乙中石墨电极上发生氧化反应 B 电流计读数为零时,反应达到化学平衡状态
B 电流计读数为零时,反应达到化学平衡状态 C 电流计读数为零后,甲乙两烧杯均加等量水稀释,电流计指针不发生偏移
C 电流计读数为零后,甲乙两烧杯均加等量水稀释,电流计指针不发生偏移 D 电流计读数为零后,在甲中再溶入FeCl2固体,乙中石墨电极为正极
D 电流计读数为零后,在甲中再溶入FeCl2固体,乙中石墨电极为正极
下列操作过程中,利用物质的氧化性的是
| A.明矾净化水 | B.纯碱除去油污 |
| C.臭氧用于餐具消毒 | D.食醋清洗水垢 |
下列物质既是电解质又能导电的是
| A.NaCl晶体 | B.液态HCl | C.熔融的KNO3 | D.Na2SO4溶液 |
下列叙述中正确的是
| A.含最高价元素的化合物,一定具有强氧化性 |
| B.阳离子只有氧化性,阴离子只有还原性 |
| C.失电子多的还原剂,还原性就强 |
| D.化学反应中,某元素由化合态变为游离态,此元素可能被氧化,也可能被还原 |
下列变化需要加还原剂才能实现的是
| A.MnO2→MnCl2 | B.Fe→Fe2+ | C.Cl-→Cl2 | D.SO2→H2SO3 |
某溶液中存在五种离子:NO3-、SO42-、Fe3+、H+和一种未知离子(OH-忽略不计),它们物质的量浓度之比为2∶3∶1∶3∶1,则未知离子可能为
| A.Fe2+ | B.Ba2+ | C.Cl- | D.Mg2+ |