列说法不正确的是
| A.物质发生化学反应都伴随着能量变化 |
| B.化学反应的速率和限度均可通过改变化学反应条件而改变 |
| C.可逆反应只是代表少数反应 |
| D.化学反应达到平衡状态时,正反应速率与逆反应速率相等 |
钛被称为21世纪金属。研究发现,用石墨作阳极、钛网作阴极、熔融CaF2—CaO作电解质,利用图所示装置制备金属钛。下列叙述正确的是
| A.乙装置阴极的电极反应式为 TiO2+4e-=Ti+2O2- |
| B.若不考虑能量的损失,制备24.0g 金属钛,需要消耗金属铝36.0g |
| C.甲装置工作过程中OH-向AgO/Ag极移动;乙装置工作过程中O2-向钛网移动 |
| D.乙装置中的石墨电极需要定期更换 |
五种短周期元素的某些信息如表所示:
| 元素 |
有关信息 |
| X |
最高价氧化物对应的水化物能与其气态氢化物反应生成盐 |
| Y |
M层上有3个电子 |
| Z |
短周期元素中原子半径最大的主族元素 |
| W |
其单质是淡黄色固体 |
| Q |
最高正价与最低负价代数和为6 |
下列说法正确的是
A.简单离子的半径大小顺序为:W>Q>Z>Y
B.Z单质在氧气中燃烧后的产物不能使品红溶液褪色
C.单质熔点高低的顺序为:Z>Y>X
D.Z与W元素只能形成原子个数比为2:1的化合物
下列说法不正确的是
| A.金属汞一旦洒落,必须尽可能收集起来,放在水中保存以防挥发;并将硫磺粉撒在洒落的地方,使金属汞转变成不挥发的硫化汞 |
| B.胶状沉淀和颗粒太小的沉淀不能用抽滤的原因是在快速过滤时沉淀易透过滤纸 |
| C.用移液管吸取溶液后,将移液管垂直放入稍倾斜的容器中,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管 |
| D.将水杨酸、乙酸酐和浓硫酸在锥形瓶中混合后,水浴加热,一段时间后取出锥形瓶,为使阿司匹林完全结晶需向锥形瓶中加适量的水,并将锥形瓶置于冰水浴中 |
下列说法正确的是
| A.红外光谱仪、质谱仪、核磁共振仪、紫外光谱仪和元素分析仪都是用于测定有机物结构的现代仪器 |
| B.工业上采用电解熔融氧化铝的方法冶炼铝,为了降低氧化铝的熔点,在实际生产中,向氧化铝中添加冰晶石 |
| C.化学家鲍林提出了氢键理论和蛋白质分子的螺旋结构模型,为DNA分子双螺旋结构模型的提出奠定了基础 |
| D.雾霾天气首要污染物为PM2.5(指大气中直径小于或等于2.5微米的颗粒物),PM2.5在空气中一定形成气溶胶 |
控制适合的条件,将反应2Fe3++2I- 2Fe2++I2设计成下图所示的原电池。下列判断不正确的是
2Fe2++I2设计成下图所示的原电池。下列判断不正确的是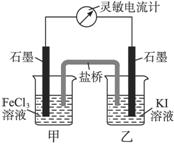

A.为证明反应的发生,可取甲中溶液加入酸性高锰酸钾溶液 |
B.反应开始时,甲中石墨电极上Fe3+被还原,乙中石墨电极上发生氧化反应 |
C.电流计读数为零时,在甲中加入FeCl2固体后,甲中石墨电极为负极 |
| D.此反应正反应方向若为放热反应,电流计读数为零时,降低温度后,乙中石墨电极为负极 |