下列离子方程式正确的是:
A.足量的乙酸与碳酸钠溶液反应:2H++CO —→CO2↑+H2O —→CO2↑+H2O |
| B.醋酸溶液与新制氢氧化铜反应: 2CH3COOH+Cu(OH)2—→Cu2++2CH3COO-+2H2O |
C.苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O 2C6H5OH+CO 2C6H5OH+CO |
| D.甲醛溶液与足量的银氨溶液共热 |
HCHO+2[Ag(NH3)2]++2OH- CO
CO +2NH
+2NH +Ag↓+3NH3+H2O
+Ag↓+3NH3+H2O
下列反应既是氧化还原反应,又是吸热反应的是()
| A.实验室制备氢气 | B.Ba(OH)2·8H2O与NH4Cl的反应 |
| C.灼热的碳与水的反应 | D.铝粉与氧化铁粉末反应 |
下面各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是()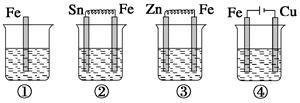
| A.②>①>③>④ | B.④>②>①>③ |
| C.④>②>③>① | D.③>②>④>① |
全球变暖给我们敲响了警钟,地球正面临巨大的挑战,下列说法不正确的是()
| A.推进小火力发电站的兴建,缓解地方用电困难,促进地方经济的快速发展 |
| B.推广“低碳经济”,减少温室气体的排放 |
| C.推广“绿色自由”计划,吸收空气中的CO2并利用廉价能源合成汽油 |
| D.利用晶体硅制作的太阳能电池可将太阳能直接转化为电能 |
电池是应用广泛的能源。
(1)设计两种类型的原电池,比较其能量转化效率。
限选材料:ZnSO4(aq),FeSO4(aq),CuSO4(aq);铜片,铁片,锌片和导线。
①完成原电池甲的装置示意图(见右图),并作相应标注。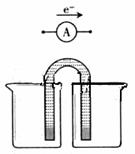
要求:在同一烧杯中,电极与溶液含相同的金属元素。
②以铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中组装原电池乙。
③甲、乙两种原电池中乙的能量转化效率较低,其原因是。
(2)Al-AgO电池可作用水下动力电源,其原理如图所示。其中的隔膜属于(填“阴”或“阳”)离子交换膜。该电池反应的化学方程式为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O,写出该电池正负极电极反应:负极,正极。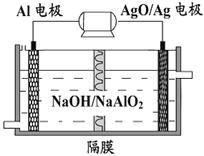
一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体VL(标准状况),向反应后的溶液中(铜元素、硫元素的存在形式分别为Cu2+、SO42-)加入足量NaOH稀溶液,产生蓝色沉淀,过滤,洗涤,灼烧沉淀,得到CuO固体12.0g,若上述气体为NO和NO2的混合物,且体积比为1﹕1,则VL可能为
| A.7.5L | B.9.5L | C.13.6L | D.16.8L |