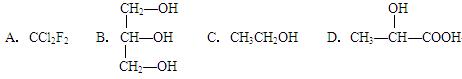已知①丙烷②正丁烷③异丁烷④2-甲基丁烷⑤己烷,上述物质的沸点按由低到高的顺序排列的是
| A.①③②④⑤ | B.⑤④③②① | C.①②③④⑤ | D.⑤①②④③ |
下列叙述中正确的是
A.除零族元素外,所有短周期元素的最高化合价在数值上都等 于该元素所属的族序数 于该元素所属的族序数 |
| B.除短周期外,其他周期均有18种元素 |
| C.副族元素中没有非金属元素 |
| D.碱金属元素是指ⅠA族的所有元素 |
A、B为短周期元素,二者可以组合成多种中学生所熟知的化合物。在这些化合物中,A与B的原子个数比为A∶B=1∶2。已知A的原子序数为n,B的原子序数是① n+2② n+3③ n+4④ n+5⑤ n+8⑥ n-5 ⑦ n-7 ⑧ n-8中的几种,其中不符合题目要求的是
A.①④ B.②⑧ C.③⑤ D.⑥⑦
共价键的断裂有均裂和异裂两种方式,即均裂:A∶B → A·+B· ;异裂:A∶B → A++[∶B]-。下列化学反应中发生共价键均裂的是
| A.2K+2H2O=2KOH+H2↑ |
| B.2Na+2C2H5OH → 2C2H5ONa+H2↑ |
C.Na2CO3+H2O NaHCO3+NaOH NaHCO3+NaOH |
D.CH3COOH+C2H5OH  H2O+CH3COOC2H5 H2O+CH3COOC2H5 |
a、b、c、d是四种短周期元素。a、b、d同周期,c、d同主族。a的原子结构示意图为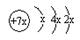 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为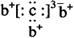 。下列比较中正确的是
。下列比较中正确的是
| A.原子半径:a>c>d>b | B.电负性a>b>d>c |
| C.原子序数:a>d>b>c | D.最高价含氧酸的酸性c>d>a |
下列化合物中含有手性碳原子的是