课外小组同学在实验室进行一氧化碳还原氧化铁的实验。
【查阅资料】
Ⅰ.常温下,甲酸(HCOOH)是无色易挥发的液体,在浓硫酸作用下易分解。甲酸分解的化学方程式为:HCOOH 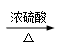 CO↑+ H2O,浓硫酸在反应中起 作用。
CO↑+ H2O,浓硫酸在反应中起 作用。
Ⅱ.铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
【实验设计及操作】
(1)利用下列装置完成用纯净、干燥的一氧化碳还原氧化铁实验,并检验气态产物。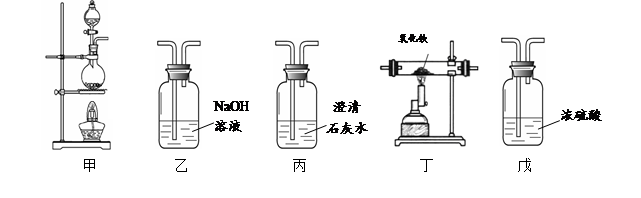
① 若各步均反应完全,装置的连接顺序为甲→→→→→尾气处理(填序号)。
② 实验时先点燃甲中的酒精灯,一段时间后再点燃丁中的酒精喷灯,目的是 ;装置乙的作用是 。
③ 装置丁中观察到的现象是 ,反应的化学方程式是 。
(2)为检验氧化铁是否反应完全,同学们设计如下实验方案:从装置丁中取出少量反应后的固体粉末于试管中,加入足量稀盐酸,若观察到有大量气泡产生且溶液变为浅绿色而非黄色,则说明氧化铁已完全反应。上述判断是否正确,理由是 。
实验室新进一批浓硝酸,化学兴趣小组为研究该试剂的保存方法,开展相关探究。请根据要求回答问题:
(1)打开盛装浓硝酸的试剂瓶,立即观察到瓶口有白雾产生。据此可知,浓硝酸具有_________(填一条物理性质)。为进一步证明浓硝酸具有该性质,兴趣小组设计如图装置(脱脂棉团因喷有稀氢氧化钠与酚酞混合液而呈红色)进行实验,实验过程中将观察到的现象是__________________,发生反应的化学方程式为_____________。
(2)将少量浓硝酸置于试管中,采用强光照射或者稍加热,立即观察到溶液上方有红棕色气体产生。据此现象可推知浓硝酸具有_________(填一条化学性质)的性质。
(3)通过上述两个实验可知,实验室应如何保存浓硝酸?__________________。
在两支试管中各加入2 mL水,然后分别加入1~2小粒碘或高锰酸钾,振荡,观察现象;然后再向两支试管中分别加1 mL汽油,振荡,静置,观察现象。记录如表所示:
| 溶剂 |
溶质 |
现象 |
| 先加水 |
碘 |
底部仍有碘固体,液体呈浅黄色 |
| 先加水 |
高锰酸钾 |
底部无固体,溶液呈深紫色 |
| 再加汽油 |
碘 |
分层,上层呈深紫色,下层近无色,底部无固体 |
| 再加汽油 |
高锰酸钾 |
分层,上层无色,下层呈深紫色,底部无固体 |
请回答:
(1)加入汽油后,投入碘的试管的上层液体名称是_________;投入高锰酸钾的试管的下层液体的名称是_____________________。
(2)从实验现象可以归纳:碘的溶解性为______________,高锰酸钾的溶解性为____________________。
(3)在科学研究中,若将大量水中溶解的少量碘“富集”起来,你认为可以采取的方法是__________________。
铁、铝、铜是常见的三种金属。同学们发现生活中的铝和铜制品表面一般不用防锈,而铁制品一般需要做防锈处理。
【提出问题】这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
【实验探究】同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格。
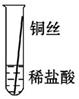
将粗细相同的铁丝、铝丝、铜丝分别插入体积相同、溶质质量分数也相同的稀盐酸中:
| 操作 |
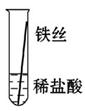 |
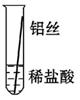 |
 |
根据现象得出金属活动性顺序 |
| 片刻后现象 |
有少量气泡 |
无气泡 |
无气泡 |
Fe>Al,Fe>Cu |
| 几分钟后现象 |
有少量气泡 |
有大量气泡 |
无气泡 |
【讨论交流】为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表面致密的氧化膜会先与盐酸反应。
【反思评价】做金属性质实验时需将金属进行打磨,打磨的目的是________。
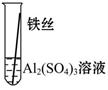
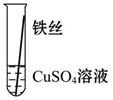
【实验验证】为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
| 操作 |
 |
 |
根据现象得出金属活动性顺序 |
| 现象 |
无明显现象 |
Al>Fe>Cu |
写出铁与硫酸铜溶液反应的化学方程式_________________。
【拓展迁移】(1)若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插入顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序。金属丝的插入顺序为________________。
(2)金属被人类大规模开发利用的大致年限也与金属活动性顺序有关,请写出铁、铝、铜三种金属材料被人类利用的先后顺序________________。
下面是对铁的锈蚀条件的探究。因通常实验中铁生锈所需要时间较长,某实验小组设计了如图所示的改进实验。
(1)检查装置的气密性:连接好装置,关闭分液漏斗的旋塞,将C导管接入到装有水的烧杯中,微热甲装置,说明气密性良好的现象是___________________。
(2)反应开始后,甲装置中的反应现象:_______________________,MnO2的作用:__________________。
(3)4分钟后观察:A处铁丝依然光亮,B处铁丝表面灰暗,D处铁丝依然光亮,A、B处实验现象对比,可得出铁生锈与____________有关;B、D处实验现象对比说明:决定铁生锈快慢的一个重要因素是________________________。
某研究性学习小组学习了工业“侯氏制碱法”的原理后,知道如下反应:
NaCl + NH3 + CO2 + H2O = NaHCO3↓+ NH4Cl。
【提出问题】能否在实验室模拟“侯氏制碱法”制取NaHCO3的过程呢?
【实验验证】如下图是该学习小组进行模拟实验时所用到的部分主要装置和药品。
请回答下列问题:
⑴ 检验A装置气密性的方法是:塞紧带长颈漏斗的橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水后,若,说明装置不漏气。
⑵该实验中用B装置制取的气体是(填化学式),B装置中盛装浓氨水的仪器名称为,本实验中使用该仪器的优点是。
⑶D是连接在装置A与装置C之间的气体净化装置,进气口是(填a或b),D的作用是除去HCl气体,反应的化学方程式为。
⑷实验时先向饱和NaCl溶液中通入较多的NH3(溶液显碱性),再通入足量的CO2,其原因是 (填写序号)。
① 使CO2更易被吸收② NH3比CO2更易制取③ CO2的密度比NH3大
⑸用的方法将生成的NaHCO3晶体从混合物中分离出来。
【得出结论】利用“侯氏制碱法”在实验室可以制取NaHCO3 。