在恒容的密闭容器中,下列反应分别达到平衡后,有关说法正确的是( )
A.2HI(g) H2(g)+I2(g);DH>0,若降低温度,颜色加深,压强增大 H2(g)+I2(g);DH>0,若降低温度,颜色加深,压强增大 |
B.2NO2(g) N2O4(g);DH<0,充入氩气,压强增大,红棕色变浅 N2O4(g);DH<0,充入氩气,压强增大,红棕色变浅 |
C.2SO2(g)+O2(g) 2SO3(g);DH<0,升温后,平均相对分子质量减小 2SO3(g);DH<0,升温后,平均相对分子质量减小 |
D.3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g);DH<0,加入铁后,Fe3O4将增加 Fe3O4(s)+4H2(g);DH<0,加入铁后,Fe3O4将增加 |
用100 mL 0.2 mol ∕ L BaCl2溶液恰好可使相同体积的Na2SO4、Al2(SO4)3、KAl(SO4)2的溶液中的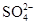 完全转化为BaSO4沉淀,需要三种盐溶液的溶质的物质的量浓度之比为()
完全转化为BaSO4沉淀,需要三种盐溶液的溶质的物质的量浓度之比为()
| A.6:2:3 | B.3:2:2 | C.3:2:1 | D.1:2:3 |
V L硫酸铝溶液中含有 m g,则Al3+的物质的量浓度为()
m g,则Al3+的物质的量浓度为()
A.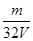 mol/L mol/L |
B.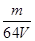 mol/L mol/L |
C.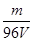 mol/L mol/L |
D. mol/L mol/L |
在无色透明的强酸性溶液中能大量共存的离子组是()
A.Ca2+ Na+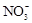  |
B.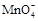 K+ K+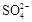 Na+ Na+ |
C.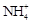 Na+ Na+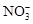 Cl– Cl– |
D.Ba2+Mg2+ Cl– |
下列反应既是氧化还原反应又是离子反应的是()
| A.用CO还原氧化铁来炼铁 | B.用锌和稀盐酸反应制氢气 |
| C.用稀硫酸除铁锈 | D.CO2通入澄清石灰水变浑浊 |
下列物质中,既能与强酸反应,又能跟强碱反应的是()
①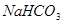 ②
②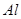 ③
③ ④
④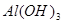 ⑤
⑤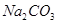
| A.①②③④⑤ | B.②③④ | C.①③④ | D.①②③④ |