实现 “节能减排” 和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
(1)关于该反应的下列说法中,正确的是____________(填字母)。
A.DH>0,DS>0 B.DH>0,DS<0 C.DH<0,DS<0 D.DH<0,DS>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
①从反应开始到平衡,CH3OH的平均反应速率
v(CH3OH) = mol·(L·min)-1;
H2的转化率 =
②该反应的平衡常数表达式K=
③下列措施中能使化学平衡向正反应方向移动的是 (填字母)。
A.升高温度 B.将CH3OH(g)及时液化抽出
C.选择高效催化剂 D.再充入l molCO2和3 molH2
(3)25℃,1.01×105Pa时,16g 液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出表示CH3OH燃烧热的热化学方程式:
(4)选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此电池的负极电极反应式
(9分)下图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。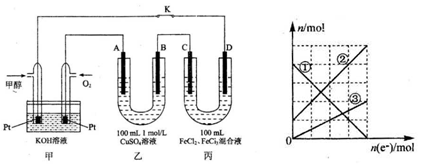
Ⅰ.工作一段时间后,断开K,此时 C电极质量减少3.2g。
(1)甲中负极的电极反应式为
(2)乙溶液此时离子浓度由大到小的顺序是
Ⅱ.连接K,继续电解一段时间,当A,B两极上产生的气体体积相同时
(3)乙中A极析出的气体在标准状况下的体积为,溶质的物质的量浓度为mol/L (不考虑溶液体积变化)
(4)丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图,则图中②线表示的是离子的变化;此时要使丙装置中金属阳离子恰好完全沉淀,需要mL 5. 0 moL/L NaOH 溶液。
(8分)氧化还原反应实际上包含氧化反应和还原反应两个过程,一个还原反应过程的离子方程式为:NO+4H++3e-===NO↑+2H2O。下列四种物质:KMnO4、Na2CO3、KI、Fe2(SO4)3中的一种物质甲,滴加少量稀硝酸,能使上述反应过程发生。
(1)被还原的元素是________;还原剂是________。
(2)写出并配平该氧化还原反应方程式:________________________________________。
(3)反应生成0.3 mol H2O,则转移电子的数目为____________。
(4)若反应后,氧化产物的化合价升高,而其他物质保持不变,则反应中氧化剂与还原剂的物质的量之比将________(填“增大”、“不变”、“减小”或“不能确定”)。
(6分)A、B、C、D、E、F六种原子序数依次增大的短周期元素。A与其余五种元素既不同周期,也不同主族;B、C、D、E、F五种元素分别位于五个相邻的主族,原子序数之和为54,其中B的单质为空气中的主要成分之一。
(1)A、B形成的化合物液态时可发生微弱电离,电离产生的阴离子的电子式为_______________。
(2)某含F的盐矿石的组成可以看作其氧化物中有1/4的F被E替换,再由D平衡其电荷形成的。该矿石的化学式为。(用氧化物形式表示)
(3)工业中制备单质E的阳极电极反应式:。
某无色溶液,由 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干离子组成,将溶液平均分为两份置于两支试管:
中的若干离子组成,将溶液平均分为两份置于两支试管:
①取其中一支试管,加入过量 。有气体生成,并得到溶液;
。有气体生成,并得到溶液;
②在①所得溶液中加入 酸化的
酸化的 ,出现白色沉淀;
,出现白色沉淀;
③取另一支试管,先加入过量的HCl酸化,再加入过量的 溶液,有气体生成同时析出白色沉淀甲,甲的质量为
溶液,有气体生成同时析出白色沉淀甲,甲的质量为 ;
;
④在③所得溶液中加入过量的 溶液,有白色沉淀乙析出。
溶液,有白色沉淀乙析出。
根据上述实验完成下列问题:
(1)溶液中一定不存在的离子是____________。
(2)一定存在的离子是________________________。
(3)判断沉淀乙成分的方法是____________________________________。
(4)写出有关反应的离子方程式
实验①:________________________________;____________________________;
(5)通过实验③可知溶液中存在的离子为________________________,原溶液中该离子的物质的量为____________。
下列框图所示的转化关系中,甲为生活中常见的金属单质,乙、丙、丁为气体单质,D为家庭中常用物质(部分反应物和生成物及溶剂水已略去)。
请回答:
(1)E的化学式为____________;甲的原子结构示意图为____________;
(2)反应①的离子方程式为____________________________________;
反应②的化学方程式为____________________________________;
(3)实验室制取并收集B的操作中,用____________法收集B,验证B已收集满的方法是_______________________________________________(限答一种)。
(4)实验室制备丁的方程式为____________________________________,工业上输送丁的管道出现气体泄漏,如何查漏(用方程式表示)______________________。