工业上以黄铁矿(主要成分FeS2,杂质不含硫元素)为原料生产硫酸。其反应原理为:①FeS2与O2高温下反应生成SO2;②SO2在催化剂作用下与O2反应生成SO3;③SO3与H2O反应生成H2SO4。试回答以下问题:
⑴生产中的尾气未经处理,排放到空气中会引起的环境问题是 。
⑵FeS2中硫元素的质量分数为 。
⑶若1.00 t SO2与O2的混合气体中,含SO2 0.40 t。在一定条件下反应,有80%的SO2发生转化,则反应后SO3的质量是 ,反应后混合气体中SO3的质量分数是 。
⑷若上述SO3与H2O完全反应,可生产98%浓硫酸多少吨?(计算过程写在答题卡上)
为测定某纯碱(Na2CO3)样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取 6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出)。产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算:
6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出)。产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算:
⑴ A点产生气体的质量m为▲;
⑵ 试样中碳酸钠的质量分数(结果精确到0.1%);
⑶ B点时,烧杯内溶液中溶质的化学式▲。
(14分)小奇同学在实验室开放日做了氧化铜和稀硫酸反应的实验后,发现实验桌上有一瓶标签残缺(如左下图所示)的NaOH溶液。为了测定此溶液的溶质质量分数,他决定利用氧化铜和稀硫酸反应后的废液。他将废液过滤,然后取100g滤液,慢慢滴加此NaOH溶液,加入NaOH溶液的质量与生成沉淀质量的关系如右下图所示:
(1)计算100g滤液中CuSO4的质量;
(2)计算此氢氧化钠溶液中溶质的质量分数。
实验室有一瓶未知浓度的BaCl2溶液,某同学取出150g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液。反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图甲所示。已知:BaCl2+Na2CO3=BaCO3↓+2NaCl请计算:
(1)配制26.5%的Na2CO3溶液80g,需要Na2CO3固体多少 g。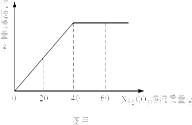
(2)BaCl2溶液的溶质质量分数是多少?(写出计算过程,结果保留到0.1%)
化学课外活动小组的同学在实验室测定某电镀厂所用CuSO4溶液中溶质的质量分数。取该CuSO4溶液50 g向其中加入某未知溶质质量分数的NaOH溶液40 g,二者恰好完全反应,生成Cu(OH)2沉淀4.9 g。
(1)计算CuSO4溶液中溶质的质量分数。
(2)根据质量守恒定律分析:反应后所得溶液的质量= g。
我国是世界钢铁产量最大的国家,炼铁的主要原料是铁矿石。用赤铁矿石(主要成分为Fe2O3)炼铁的反应原理为: 3CO+ Fe2O3高温2Fe + 3CO2 。
(1)上述反应不是置换反应的理由是?
(2)Fe2O3中铁元素的质量分数是?
(3)根据化学方程式计算:用含Fe2O360%的赤铁矿石800 t,理论上可炼出纯铁多少吨?