巴豆酸的结构简式为CH3—CH=CH—COOH。现有 ①氯化氢、②溴水、③纯碱溶液、④乙醇、⑤酸性高锰酸钾溶液,试根据巴豆酸的结构特点,判断在一定条件下,能与巴豆酸反应的物质是( )。
| A.只有②④⑤ | B.只有①③④ | C.只有①②③⑤ | D.①②③④⑤ |
下列说法正确的是
| A.中和等体积、等物质的量浓度的盐酸和醋酸所消耗的NaOH的物质的量相等 |
| B.若NaHA溶液的pH<7,则H2A一定是强酸 |
| C.将NaOH溶液加入到NH4Cl溶液至中性时,溶液中c(NH4+)=c(Cl一) |
| D.常温下,将pH=11的Ba(OH)2溶液加水稀释10倍后,溶液的pH=12 |
T℃时,某浓度醋酸钠溶液的pH=10,下列说法一定正确的是
| A.溶液中由水电离出的OH一离子浓度c(OH一)=1×10一10mol/L |
| B.溶液中存在:c(H+)·c(OH一)=l×10-14(mol/L)2 |
| C.溶液中存在:c(Na+)>c(CH3COO一)>c(OH一)>c(H+)>c(CH3COOH) |
| D.溶液中存在:c(CH3COOH)+c(CH3COO一)=c(Na+) |
向密闭容器中充入物质A和B,发生反应aA(g)+bB(g)  cC(g)。反应过程中,物质A的含量(A%)和C的含量(C%)随温度(T)的变化曲线如图所示,下列说法正确的是
cC(g)。反应过程中,物质A的含量(A%)和C的含量(C%)随温度(T)的变化曲线如图所示,下列说法正确的是
| A.该反应在T1、T3温度时达到过化学平衡 |
| B.该反应在T2温度时达到过化学平衡 |
| C.该反应的逆反应是放热反应 |
| D.升高温度,平衡会向正反应方向移动 |
甲和乙两烧杯中各装有100mL 0.2mol/LAlCl3溶液,向两烧杯中分别加入相同体积、相同浓度的NaOH溶液和氨水,两烧杯中都有沉淀生成。下列判断正确的是
| A.实验过程中甲中和乙中的现象始终保持一致 |
| B.甲中沉淀一定比乙中的少 |
| C.甲中沉淀可能比乙中的多 |
| D.乙中沉淀可能比甲中的多 |
五种短周期元素在周期表中的位置如图所示,其中Z元素原子的最外层电子数等于电子层数。下列判断正确的是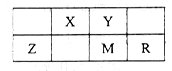
| A.Z的氧化物可以做光导纤维 |
| B.气态氢化物稳定性:M>R |
| C.最高价氧化物对应水化物的酸性:Y>X |
| D.Z、M、R的原子半径依次增大,最高化合价依次升高 |