下列各组化合物中,化学键类型完全相同的是
| A.CaCl2和 Na2S | B.Na2O 和Na2O2 | C.CO2和CaO | D.HCl和NaOH |
量取10mL碘的饱和水溶液,倒入分液漏斗中,然后再注入4mL四氯化碳,用力振荡后静置,实验现象为
| A.液体分层,上层为四氯化碳层,黄色 |
| B.液体分层,上层为水层,紫色 |
| C.液体分层,下层为四氯化碳层,紫色 |
| D.液体分层,下层为水层,黄色 |
检验某未知溶液中时否含有SO42-,下列操作最合理的是
| A.加入稀硝酸酸化的Ba(NO3)2溶液 |
| B.加入盐酸酸化的BaCl2溶液 |
| C.先加盐酸酸化,再加BaCl2溶液 |
| D.先加BaCl2溶液,在加稀硝酸 |
下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是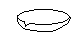
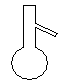
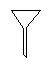
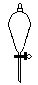
| A.蒸馏、蒸发、萃取、过滤 | B.过滤、蒸发、萃取、蒸馏 |
| C.萃取、过滤、蒸馏、蒸发 | D.蒸发、蒸馏、过滤、萃取 |
下列实验操作中正确的是
| A.应使混合物中的水分完全蒸干后,才能停止加热 |
| B.分液操作时,下层液体从分液漏斗下口放出后再将上层液体从下口放出到另一个烧杯中 |
| C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
| D.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
一定温度下,在三个体积均为2.0 L的恒容密闭容器中发生如下反应:PCl5(g)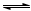 PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
| 编号 |
温度(℃) |
起始物质的量 (mol) |
平衡物质的量 (mol) |
达到平衡所需时间 (s) |
|
| PCl5(g) |
PCl3(g) |
Cl2(g) |
|||
| Ⅰ |
320 |
0.40 |
0.10 |
0.10 |
t1 |
| Ⅱ |
320 |
0.80 |
t2 |
||
| Ⅲ |
410 |
0.40 |
0.15 |
0.15 |
t3 |
下列说法正确的是
A.平衡常数K:容器Ⅱ>容器Ⅲ
B.反应到达平衡时,PCl5的转化率:容器Ⅱ<容器Ⅰ
C.反应到达平衡时,容器I中的平均速率为v(PCl5)= 0.10/t1 mol/(L·s)
D.起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl3 0.45 mol和Cl2 0.10 mol,则反应将向逆反应方向进行