关于苯的说法正确的是
| A.苯使溴水褪色是因为发生了取代反应 |
| B.苯中各原子均在同一平面. |
| C.苯中没有典型的碳碳双键,所以不能发生加成反应. |
| D.苯中的含碳量高,燃烧时产生大量的黑烟. |
下列关于氧化物的叙述中不正确的是
①酸性氧化物均可与水反应生成相 应的酸②非金属氧化物肯定是酸性氧化物
应的酸②非金属氧化物肯定是酸性氧化物
③碱性氧化物肯定是金属氧化物④金属氧化物都是碱性氧化物
⑤不能跟酸反应的氧化物一定能跟碱反应
| A.①②④⑤ | B.①②③④⑤ | C.②③④ | D.③⑤ |
下列说法正确的是
| A.根据丁达尔现象可以区分食盐水和硫酸铜溶液 |
| B.某离子被沉淀完全是指该离子在溶液中的浓度等于0 |
| C.在任何条件下,纯水都呈中性 |
| D.水的离子积常数Kw随温度、外加酸(碱)浓度的改变而改变 |
下列叙述正确的是
| A.元素的化学性质主要决定于原子的核外电子数 |
| B.氯化氢溶于水能导电,但液态氯化氢不能导电 |
C.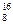 O、 O、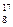 O和 O和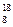 O互为同位素,均属于氧元素,且性质相同 O互为同位素,均属于氧元素,且性质相同 |
| D.导电性强的溶液里自由移动的离子数目一定比导电性弱的溶液里自由移动的离子数目多 |
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,生成4mol z时放出热量Q KJ, 它们的物质的量随时间的变化如表所示。
| t/min |
X/mol |
Y/mol |
Z/mol |
| 0 |
1.00 |
1.00 |
0.00 |
| 1 |
0.90 |
0.80 |
0.20 |
| 3 |
0.75 |
0.50 |
0.50 |
| 5 |
0.65 |
0.30 |
0.70 |
| 9 |
0.55 |
0.10 |
0.90 |
| 10 |
0.55 |
0.10 |
0.90 |
| 14 |
0.55 |
0.10 |
0.90 |
(1)根据上表中数据,在答卷该题相应位置上画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
(2) 写出体系中发生反应的热化学方程式 ______;
(3) 列式计算该反应在0-3min时间内产物Z的平均反应速率:
(4) 该反应达到平衡时反应物X的转化率 等于______________________;
等于______________________;
(5) 改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线1、2、3(如下图所示)则曲线1、2、3所对应的实验条件改变分别是:1 _____2_____3_____的曲线: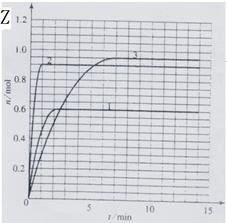
将体积都为10 mL、pH都等于3的醋酸和盐酸,加水稀释至a mL和b mL,测得稀释后溶液的pH均为5。则稀释后溶液的体积()
| A.a="b=100" mL | B.a="b=1000" mL | C.a>b | D.a<b |