A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为:,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
(1)写出下列元素的符号:A _________ D __________
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是__________,碱性最强的是_________。
(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是__________,电负性最大的元素是__________。
(4)D的氢化物比C的氢化物的沸点__________(填"高"或"低"),原因_____________ (5)A、B、C最高价氧化物的晶体类型分别是______晶体、______晶体、______晶体
(5)A、B、C最高价氧化物的晶体类型分别是______晶体、______晶体、______晶体
(6)画出D的核外电子排布图___________________________________________,这样排布遵循了___________原理和____________规则。
让直径比孔穴小的分子通过而将大的分子留在外面,故又称“分子筛”。“分子筛”在表面化学中有重要作用,是重要的催化剂和催化剂载体。以高岭土(主要成分:Al2Si2O7·2H2O)、石灰石、海水为原料生产“分子筛”的工艺流程如下:
回答下列问题
(1)操作a的作用是,副产品A是;
(2)气体通入滤液中发生反应的离子方程式为、;
(3)NaOH和不溶物在适当温度下发生的化学反应方程式为、
;
(4)高岭土主要成分的化学式可表示为Al2O3·2SiO2·2H2O,则分子筛的化学式也可表示为。
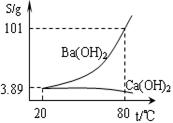
实验室有一份混有少量碳酸钙杂质的碳酸钡样品。分离并提纯碳酸钡的实验步骤如下,请根据要求填空(右图为Ba(OH)2和Ca(OH)2的溶解度曲线):







(1)高温灼烧碳酸钡和碳酸钙的混合物,直至分解分解。
所需仪器除坩埚、泥三角、玻璃棒、三脚架外还有
;
(2)将灼烧后的固体混合物置于80℃的热水中,制成氢氧化钡的热饱和溶液。为减少Ba(OH)2的损失并除去不溶物应进行的操作是;
(3)将“⑵”中滤液并过滤,得到的Ba(OH)2固体溶于水制成溶液。
(4)向制得的Ba(OH)2溶液中滴加(填一种试剂名称),再通入二氧化碳。当观察到时,即可停止通二氧化碳。
(5)滤出碳酸钡沉淀,经洗涤、干燥后即得到纯净的碳酸钡。
过碳酸钠(Na2CO4)和稀硫酸反应的化学方程式为:2Na2CO4 +2H2SO4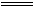 2Na2SO4+O2↑+2H2O+2CO2↑
2Na2SO4+O2↑+2H2O+2CO2↑
某过碳酸钠样品中含有少量Na2O2,甲、乙两位同学各称质量为mg的该样品,选用下图所示的仪器组合成测定样品的纯度的装置。仪器的连接顺序,甲是①⑦③⑥④;乙是①②。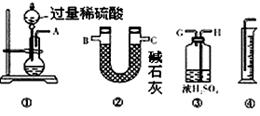
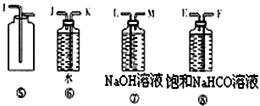
(1)甲同学想通过实验测得的数据是。他连接装置的顺序存在错误,调整的方法是。
(2)乙同学想通过实验测得的数据是。按他测得的数据计算出来的实验结果(填“偏高”、“偏低”或“无影响”),理由是。
(3)为了测得准确的实验数据,请你将乙同学的实验装置进行改进,写出各接口的连接顺序:。
(4)按你改进的实验装置进行实验,若测得实验前后装置②的质量分别是W1g和W2g,则样品中过碳酸钠的质量分数为。
(1)钟乳石和石笋的主要成分是碳酸钙,其形成过程如右图所示。随着旅游人数的增加,潮湿溶洞中的钟乳石和石笋受到二氧化碳侵蚀,其化学方程式为:__________________________________。
(2)某学生提出一个修复溶洞底部受损石笋的研究方案,由以下五步组成,正确的实验步骤依次是__________。
①将盛有碱溶液的容器置于石笋的上部②配制一定浓度的碱溶液③选择合适的碱④调节碱溶液下滴的速度⑤观察石笋表面复原情况
锗是ⅣA族元素,它的单质晶体是一种良好的半导体材料,广泛用于电子工业,锗可以从燃烧的烟道灰中提取,其过程如下: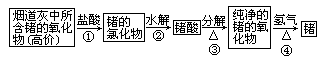
试写出上述过程中①、③、④步反应的化学方程式。
①_________________;
③_________________;
④_________________;