生活中处处有化学。请用下列物质的化学式填空:
①小苏打 ②生石灰 ③盐酸 ④熟石灰 ⑤硝酸钾 ⑥碳酸钙
| A.常用作食品干燥剂的是; | B.可用作补钙剂的是; |
| C.常用来改良酸性土壤的碱是; | D.可用作复合肥的是; |
E.胃液中可帮助消化的是 ;F.常用作发酵粉的是 。
右图是有关氧气的知识网络图(条件略),请填空: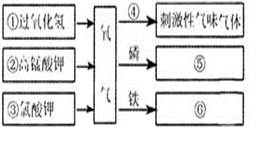
(1)物质的化学符号为⑤⑥。
(2)得到物质④的反应表达式:;属于反应(填化合或分解,下同)
(3)由①反应制取氧气的反应表达式:;属于反应
(1)2010年世博会5月1日在我国上海开幕。下列设计或活动能体现“低碳”理念的是。
| A.用牛奶等废弃饮料纸包装制成环保椅、环保垃圾桶和节目册等 |
| B.利用老厂房进行改造成宝钢大舞台、船坞等重要演出场地 |
| C.世界自然基金会(WWF)于6月5日举办音乐会,演出过程中 “熄灯一小时”,这一小时演出舞美所需电力均由太阳能蓄电池供电。 |
| D.中国国家馆所有的门窗都采用LOM-E玻璃,将阳光转化为电能并储存起来,为建筑外墙照明提供能量 |
E.超过1000辆的新能源汽车服务于世博
(2)“低碳”生活、人人有责。如果你想去上海参加世博会,请你在交通、餐饮、生活等方面提出一条符合“低碳”理念的做法:。
黄金(Au)饰品分为千足金和K金等。千足金的含金量接近99.9%。K金通常有黄、红、白色之分,其中白色K金实际上是黄金与镍、锌、铜等元素的合金。根据国家标准,K代表含金量,24K金的含金量理论值是100%。
(1)18K金中,金的质量分数约是。
(2)根据合金与其成分金属在硬度与熔点方面的一般规律分析,24K金与18K金相比,熔点较低的是;硬度较小的是。
(3)黄金可以制成金戒指、金耳环、金项链等形态各异的金饰品,说明金具有良好的性。
目前世界上年产量最高的金属是铁,它的两种主要合金是 和;它们的主要区别是不同,用它们做饮具是利用了其。
下图是A、B、C三种固体物质的溶解度曲线,试看图后回答: 
① 在t3℃时,三种物质的溶解度从小到大的顺序是:;
② 在时,B与C的溶解度相等;
③ 物质C的溶解度随温度升高而;
④要从A、B、C的混合物中分离出C,最好用法。