在某温度下,H2和I2各0.10mol的气态混合物充入10L的密闭容器中,发生反应:H2(g)+I2(g) 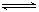 2HI(g),充分反应后达到平衡,测得c(H2)="0.008" mol•L-1,则该反应的平衡常数为( )
2HI(g),充分反应后达到平衡,测得c(H2)="0.008" mol•L-1,则该反应的平衡常数为( )
| A.40 | B.62.5 | C.0.25 | D.4 |
已知:(1)Zn(s)+ 1/2O2(g)==ZnO(s)ΔH = -348.3kJ/mol
(2)2Ag(s) +1/2 O2(g)="=" Ag2O(s) ΔH = -31.0kJ/mol
则Zn(s)+ Ag2O(s) ="=" ZnO(s) + 2Ag(s) 的ΔH等于
| A.-317.3kJ/mol | B.-379.3kJ/mol | C.-332.8 kJ/mol | D.+317.3 kJ/mol |
已知在1×105 Pa,298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是
| A.H2O ( g ) = H2 ( g ) + 1/2O2 ( g )△H =" +242" kJ/mol |
| B.2H2 ( g ) + O2 ( g ) = 2H2O ( l )△H = -484 kJ/mol |
| C.H2 ( g ) + 1/2O2 ( g ) = H2O ( g )△H =" +242" kJ/mo |
| D.2H2 ( g ) + O2 ( g ) = 2H2O ( g )△H =" +484" kJ/mol |
下列叙述正确的是
| A.物质燃烧不一定是放热反应 |
| B.放热反应不需要从外界吸收任何能量就能发生 |
| C.在一个确定的化学反应中,反应物总能量总是高于生成物总能量 |
| D.化学反应除了生成新的物质外,还伴随着能量的变化 |
如图所示装置中,可观察到电流表指针偏转,M棒变粗,N棒变细。下表所列M、N、P物质中,可以组合成该装置的是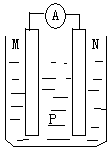
| 选项 |
M |
N |
P |
| A |
锌 |
铜 |
稀硫酸 |
| B |
铜 |
铁 |
稀盐酸 |
| C |
银 |
锌 |
硝酸银溶液 |
| D |
锌 |
铁 |
硝酸铁溶液 |
A、B、C、D四种金属分别用导线两两相连浸入电解液中组成原电池。A、B相连时,A为负极;C、D相连时,电流由D流到C;A、C 相连时,C极上有大量气泡;B、D相连时,D极发生氧化反应。据此判断四种金属的活动性顺序是
A.A>C>D>B B.D>A>B>C C.A>D>C>B D.C>B>A>D