已知1g氢气燃烧生成液态水时放出142.9KJ热量,则反应的热化学方程式为
A.H2(g) +  O2(g) ="=" H2O(l);△H= —142.9kJ/mol O2(g) ="=" H2O(l);△H= —142.9kJ/mol |
| B.2H2(g) + O2(g) ="=" 2H2O(l);△H= 571.6kJ/mol |
| C.2H2(g) + O2(g) ="=" 2H2O(l);△H= —571.6kJ/mol |
| D.2H2 + O2 ="=" 2H2O;△H= —571.6kJ |
下列对化学知识概括合理的是( )
| A.酸性氧化物都是非金属氧化物 |
| B.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物 |
| C.丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应 |
| D.熔融状态能导电的物质一定是离子化合物 |
用下面的方案进行某些离子的检验,其中方案设计得最严密的是()
A.检验试液中的SO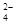 :试液 :试液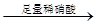 无沉淀 无沉淀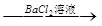 白色沉淀 白色沉淀 |
B.检验试液中的Fe2+:试液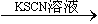 无明显现象 无明显现象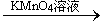 红色溶液 红色溶液 |
C.检验试液中的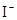 :试液 :试液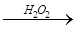 棕黄色溶液 棕黄色溶液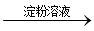 蓝色溶液 蓝色溶液 |
D.检验试液中的CO :试液 :试液 白色沉淀 白色沉淀 沉淀溶解 沉淀溶解 |
X、Y、Z、W是中学化学常见的四种物质,它们之间具有如图所示转化关系,则下列组合不可能的是()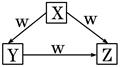
| X |
Y |
Z |
W |
|
| A |
C |
CO |
CO2 |
O2 |
| B |
Na |
Na2O |
Na2O2 |
O2 |
| C |
AlCl3 |
Al(OH)3 |
NaAlO2 |
NaOH |
| D |
Fe |
FeCl2 |
FeCl3 |
Cl2 |
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如下图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为()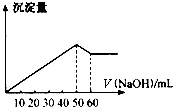
| A.6:1 | B.3:1 |
| C.2:1 | D.1:2 |
浓度均为0.1mol·L—1的三种溶液等体积混合,充分反应后没有沉淀的一组溶液是()
| A.BaCl2、 NaOH 、 NaHCO3 | B.Na2CO3、MgCl2、H2SO4 |
| C.AlCl3、NH3·H2O 、NaOH | D.Ba(OH)2、CaCl2、Na2SO4 |