下列有关叙述正确的是( )
| A.同系物间有相似的化学性质 |
| B.同分异构体间有相似的化学性质 |
| C.分子组成上相差一个“CH2”原子团的两种有机物必定互为同系物 |
| D.相对分子质量相等的两种有机物必定是同分异构体 |
在含有KCI和KI的混合液中,滴入足量的溴水,待反应完全后,将溶液蒸干、灼烧,最后得到的残留固体物质为
| A.KCI和KBr | B.KCI、KBr和I2 | C.KBr | D.KBr和KI |
将一定量的镁和铝分别与足量的盐酸反应,若放出氢气的质量相等,则参加反应的镁和铝的物质的量之比为
| A. 1:1 | B.2:3 | C.3:2 | D.8:9 |
玻璃器皿上沾有一些用水洗不掉的下列残留物,其洗涤方法正确的是
①残留在试管内壁上的碘,用酒精洗涤
②盛放过苯酚的试剂瓶中残留的苯酚,用酒精洗涤
③做银镜反应后残留的银,用稀氨水洗涤
④沾附在试管内壁上的油脂,用热碱液洗涤
| A.①②④ | B.②③④ | C.①③④ | D.①②③④ |
生石灰中可能含有CaCO3和SiO2杂质,若要检验是否存在这两种杂质,最适宜的试剂是
| A.浓硫酸 | B.氢氧化钠溶液 | C.水 | D.盐酸 |
下列反应不属于取代反应的是
A.CH4+Cl2 CH3Cl+HCl CH3Cl+HCl |
B.CH3CH2OH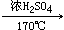 CH2= CH2+H2O CH2= CH2+H2O |
C. +Br2 +Br2  |
D. |