甲酸、乙酸、碳酸、苯酚的酸性由强到弱的顺序是( )
| A.碳酸、苯酚、甲酸、乙酸 | B.甲酸、乙酸、碳酸、苯酚 |
| C.甲酸、碳酸、苯酚、乙酸 | D.苯酚、碳酸、乙酸、甲酸 |
已知:2Zn(s)+O2(g)===2ZnO(s) ΔH=-701.0 kJ·mol-1
2Hg(l)+O2(g)===2HgO(s) ΔH=-181.6 kJ·mol-1
则反应Zn(s)+ HgO(s)===ZnO(s)+ Hg(l)的ΔH为( )
| A.+519.4 kJ·mol-1 |
| B.+259.7 kJ·mol-1 |
| C.-259.7 kJ·mol-1 |
| D.-519.4 kJ·mol-1 |
下列热化学方程式或离子方程式中,正确的是( )
| A.甲烷的标准燃烧热为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)===CO2(g)+2H2O(g)ΔH=-890.3 kJ·mol-1 |
B.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)  2NH3(g) ; ΔH=-38.6 kJ·mol-1 2NH3(g) ; ΔH=-38.6 kJ·mol-1 |
| C.氯化镁溶液与氨水反应:Mg2++2OH-===Mg(OH)2↓ |
D.氧化铝溶于NaOH溶液:Al2O3+2OH-===2AlO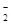 +H2O +H2O |
已知热化学方程式:
2H2(g)+O2(g)===2H2O(g) ΔH1=-483.6 kJ/mol
则对于热化学方程式:
2H2O(l)===2H2(g)+O2(g) ΔH2
下列说法正确的是( )
| A.热化学方程式中化学计量数表示分子个数 |
| B.该反应的ΔH2=+483.6 kJ/mol |
| C.|ΔH2|<|ΔH1| |
| D.|ΔH2|>|ΔH1| |
已知:2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1,
Na2O2(s)+CO2(g)===Na2CO3(s)+ O2(g)ΔH=-226 kJ·mol-1。
O2(g)ΔH=-226 kJ·mol-1。
根据以上热化学方程式判断,下列说法正确的是( )。
| A.CO的燃烧热为283 kJ |
| B.下图可表示由CO生成CO2的反应过程和能量关系 |
| C.2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g)ΔH>-452 kJ·mol-1 |
| D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023 |
下列与化学反应能量变化相关的叙述正确的是( )。
| A.生成物总能量一定低于反应物总能量 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同 |