把aL含硫酸铵和硝酸铵的混合溶液分成两等份,一份需用bmol烧碱刚好把氨气全部赶出,另一份与氯化钡反应时,消耗BaCl2 cmol,则原溶液中NO3-的物质的量浓度是
| A.(b-2c)/a mol/L | B.(2b-c)/a mol/L |
| C.(2b-2c)/a mol/L | D.(2b-4c)/a mol/L |
海带中含碘元素,有人设计如下步骤来提取碘:
①通适量Cl2;②将海带烧成灰,向灰中加水搅拌;③加CCl4振荡;④过滤;⑤用分液漏斗分液。正确的步骤顺序是
| A.①③⑤②④ | B.②④③①⑤ | C.②④①③⑤ | D.③①②⑤④ |
对于反应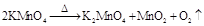 ,下列说法错误的是
,下列说法错误的是
| A.氧化剂和还原剂都是KMnO4 |
| B.该反应的还原产物只有MnO2 |
| C.该反应的氧化产物是O2 |
| D.KMnO4中Mn元素表现氧化性,O元素表现还原性 |
NaF、NaI、MgO均为离子化合物,现有下列数据,试判断三种化合物的熔点、沸点高低的顺序是
| 物质 |
①NaF |
②NaI |
③MgO |
| 离子电荷数 |
1 |
1 |
2 |
| 离子的核间距 |
23.1nm |
31.8nm |
21.0nm |
A.①>②>③B.③>②>①C.③>①>②D.②>①>③
已知一个SO2分子的质量为n kg,一个SO3分子的质量为m kg(设两种分子中S、O原子分别具有相同的中子数),若以硫原子质量的1/32作标准,SO2的相对分子质量为
A. |
B.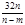 |
C. |
D. |
反应A+B→C分两步进行:①A+B→X;②X→C。反应过程中能量变化如图所示。下列有关叙述正确的是
A.E2表示反应X→C的反应热
B.A+B→C此反应放热
C.X是反应A+B→C的催化剂
D.加入催化剂可改变反应A+B→C的反应热