工业上可以用食盐和石灰石为原料制取纯碱(Na2CO3),生产的关键是在沉淀池中让NaCl、NH3、CO2和H2O尽可能多地转化成NaHCO3(固体沉淀物)和NH4Cl(溶液)。主要生产流程如下:(已知2NH4Cl+Ca(OH)2=CaCl2+2NH3 ↑+2H2O)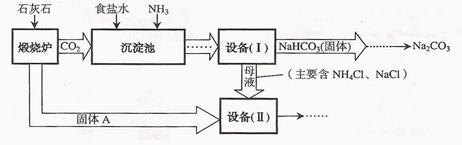
(1)“煅烧炉”中发生反应的化学方程式是 。
(2)若在化学实验室里分离“设备(I)”中的混合物,用到的操作名称是 ,该操作中用到的玻璃仪器有烧杯、 和 。
(3)在“设备(Ⅱ)”中固体A与水反应的化学方程式是 。
(4)对“设备(Ⅱ)”中的母液处理后,除水以外可在本流程中再利用的物质有 (填写化学式)。
(5)请写出纯碱(Na2CO3)的一点用途:
(9分)化学来源于生活,应用于生活。用化学知识回答下列问题:
(1)某些食品包装袋内常用铁粉作“双吸剂”,以防止食品腐败,其主要作用是吸收空气中的。
(2)若要验证铜、铁、铝的活动性顺序,某同学已经选择了打磨过的铁丝,你认为他还需要的另外两种溶液是、。
(3)液态的植物油和固态的动物脂肪合称为油脂,其含有元素。若锅里的油着火了,可采取的灭火措施是。
(4)硫酸钠是制造纸浆、染料稀释剂、医药品等的重要原料。某硫酸钠粗品中含有少量CaCl2和MgCl2,实验室进行提纯的流程如下: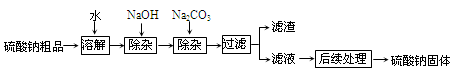
回答下列问题:
①溶解过程需要的玻璃仪器有烧杯和____________。
②用NaOH除杂时,反应的化学方程式为___________________________。
③NaOH和Na2CO3如果添加过量了,可加入适量溶液除去。
④“后续处理”的主要操作是蒸发,为了获得纯净的硫酸钠,应蒸发至_____(填序号)。
A.完全蒸干时停止加热
B.有较多固体析出时停止加热,利用余热蒸干
C.有大量固体析出时停止加热,过滤弃去剩余的少量溶液
(4分)甲、乙、丙三种固体物质的溶解度曲线如下图所示。
(1)甲的溶解度为20 g时对应的温度为;
(2)t3℃时甲、乙饱和溶液中溶质质量分数的大小关系是甲乙(填“大于”、“小于”或“等于”)。
(3)乙的饱和溶液中含有少量的甲,由该液体得到固体乙采用的方法是。
(4)下列说法正确的是。
| A.从t1℃升温到t3℃,甲、丙的饱和溶液都会析出晶体 |
| B.常温下加水稀释丙的饱和溶液,需要用到的仪器有: 烧杯、玻璃棒、量筒、胶头滴管 |
| C.t2℃乙的饱和溶液中加入固体乙,溶质的质量分数不变 |
| D.t3℃等质量甲、乙、丙的饱和溶液中,含溶质最多的是丙 |
碳元素是组成许多物质的基本元素。
(1)甲烷(CH4)是一种清洁能源。在甲烷中碳氢元素质量比,0.1mol含有个甲烷分子,质量为g。写出甲烷完全燃烧的化学方程式。
(2)分析下表,与煤相比,用天然气作燃料的优点有。
| 1g物质完全燃烧 |
||
| 产生二氧化碳的质量/g |
放出的热量/kJ |
|
| 甲烷 |
2.75 |
56 |
| 碳 |
3.67 |
32 |
(3)为提高煤的利用率,可将其转化为可燃性气体,该反应的微观示意图如下,则生成物的分子个数比为。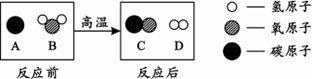
(4)化石燃料主要包括煤、和天然气。
(5)很多天然矿石中含有碳元素,菱锰矿的主要成分是碳酸锰(MnCO3),其中锰元素的化合价为。
(6)液态二氧化碳可用于扑救档案室发生的火灾,下列说法正确的是(填字母序号)。
A.液态二氧化碳汽化后不会污染档案
B.二氧化碳可覆盖在可燃物表面,隔绝空气
C.液态二氧化碳汽化时吸热,降低可燃物的着火点
(7分)通过化学学习.更理解化学使生活更美好。现有H、C、N、O、K 五种元素.请选用其中的元素写出下列物质的化学式或化学方程式。
(1)最常用的溶剂:;
(2)可做食品袋填充气体的单质;
(3)可用作化肥的盐;
(4)能供给呼吸的气体
(5)极易与血红蛋白结合的有毒气体:
(6)H、C、O是组成物质种类最多的元素,用这三种元素任写一种物质的化学式;
(7)请用上述五种元素任写一个化学方程式。
某同学用稀硫酸、氢氧化钠溶液、酚酞溶液三种试剂,按如图所示进行酸碱中和反应的实验.
①在盛有试剂Ⅰ的试管中,先后加入试剂Ⅱ、试剂Ⅲ,同时不断振荡,观察到溶液先变红后变无色。试剂Ⅱ是(8)。
②上述实验过程中:溶液的(9)减弱,这是由于(10),由此证明上述实验过程确实发生了化学反应,写出反应的化学方程式(11)。
③取上述实验后的无色溶液少许于试管中,加入合适的试剂,可验证化学反应是否恰好完全反应,下列中不能加入的试剂是(12) 。
| A.石蕊溶液 | B.铜片 | C.氧化铁 | D.硝酸钡溶液 |