纳米氧化亚铜(Cu2O)是一种用途广泛的光电材料,常用的制备方法有电化学法、湿化学法等。电化学法可用铜棒和石墨作电极,电解Cu(NO3)2稀溶液制备。湿化学法的制备过程为:在KOH溶液中加入一定量的CuSO4溶液,再加入一定量的还原剂——肼(N2H4),加热并保持温度在90℃。检验反应完全后,分离、洗涤、真空干燥得到固体样品。反应方程式为:
4CuSO4 + N2H4 + 8KOH = 2Cu2O + N2↑+ 4K2SO4 + 6H2O
⑴电化学法制备Cu2O时,铜棒做 极,阴极生成Cu2O的电极反应式为 。
⑵湿化学法中,检验纳米Cu2O已经生成的实验方法是 。
⑶湿化学法得到的产品中常含有Cu。称取某产品1.76 g(设仅含Cu2O和Cu),加入足量的稀硝酸,充分反应后得到标准状况下的NO气体224mL,计算产品中Cu2O的质量分数。(写出计算过程)
回答下列问题:
(1)目前出现的“不粘锅”、不粘油的吸油烟机等等新型厨具,其秘密就是表面有一种叫做“特富隆”的涂层,实际上就是号称“塑料王”的聚四氟乙烯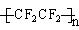 。写出由四氟乙烯在催化剂的条件下合成聚四氟乙烯的反应方程式
。写出由四氟乙烯在催化剂的条件下合成聚四氟乙烯的反应方程式
(2)NaHCO3是制作糕点的常用疏松剂。NaHCO3受热分解反应的化学方程式是:。
(3)“低碳生活”成为新的时尚流行全球,控制C02排放需要从人人做起,请你提出一种“低碳生活”的举措。
某地区使用含较少Ca2+、Mg2+的天然水按下列四个步骤制取自来水。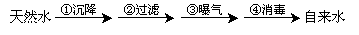
回答下列问题:
(1)该地区的天然水属于(“硬水”或“软水”)
(2)在第一步中需要加入凝聚剂,常用的凝聚剂可以是(任填一种凝聚剂名称)
(3)常用液氯作为消毒剂,其原理是
现有①氟氯烃 ②二氧化碳 ③二氧化硫 ④废弃塑料制品⑤富含氮、磷元素的污水。请你根据已有的环保知识,选择恰当的序号填空:
(1)能形成酸雨的是;(2)能破坏臭氧层的是;
(3)使水体富营养化的是;(4)导致“白色污染”的是。
蛋白质是构成`生命的基础物质。在鸡蛋、蔬菜、花生油等食物中,富含蛋白质的是。"84消毒液”在日常生活中被广泛使用。该消毒液无色,对某些有色物质具有漂白作用,它的有效成分是(填" KMnO4”或",NaClO")。
实验室制取硝基苯的主要步骤如下:
①配置一定比例的浓硫酸和浓硝酸的混合物,加入反应器
②向室温下的混合液中逐滴加入一定量的苯,充分振荡,混合均匀
③在50-60℃条件下发生反应,直到反应结束
④除去混合酸后,粗产品依次用蒸馏水和5﹪NaOH溶液洗涤,最后用蒸馏水洗涤
⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏得到纯硝基苯
填写下列空白:
①配置一定比例的浓硫酸和浓硝酸的混合液时,操作注意事项是
②步骤③中,为了使反应在50-60℃下进行,常用的方法是。
③步骤④中洗涤、分离粗硝基苯使用的仪器是。
④步骤④中粗产品用5﹪NaOH溶液洗涤的目的是。
⑤此反应可表示为。