物质的量浓度都为0.1 mol/L的下列溶液中,pH最小的是
| A.NH4Cl | B.NaCl | C.CH3COONa | D.NaNO3 |
常温下,由水电离出的c(H+)=1×10 -14 mol/L的溶液中,一定能大量共存的离子组是
-14 mol/L的溶液中,一定能大量共存的离子组是
()
| A.K+、Ba2+、NO3- | B.Ca2+、Al3+、Br- |
| C.Na+、ClO-、SO42- | D.Mg2+、Cl-、NH4+ |
下列反应的离子方程式正确的是 ()
()
A.向苯酚钠溶液中通往少量二氧化碳:CO2+H2O+2C6H5O- 2C6H5OH+CO32- 2C6H5OH+CO32- |
| B.向氯化铝溶液中加入过量氢氧化钾溶液:Al3++4OH- |
| C.向小苏打溶液加入甲酸溶液:HCO3-+H+ |
| D.向溴化亚铁溶液中通往过量氯气:Fe2++2Br-+2Cl2 |
国际奥委会公布的违禁药物有138种,其中某种兴奋剂分子结构如图。关于它的说法正确的是()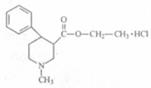
| A.该物质属于芳香烃 |
| B.该分子中所有碳原子共面 |
| C.1 mol 该物质与氢氧化钠溶液完全反应,最多消耗2 mol NaOH |
| D.该物质的化学式为C15H24ClNO2 |
下列说法不正确的是()
| A.SO2、Na2O2、活性炭都能使品红溶液褪色,但原理不同 |
| B.非金属氧化物不一定是酸性氧化物,但大多数金属氧化物为碱性氧化物 |
| C.具有相同分子数的甲酸性氧化物,但大多数金属氧化物为碱性氧化物 |
| D.同温同压下,3 molC2H2(g)和1 mol C6H6(g)的密度相等 |