钙元素对人类生命和生活具有重要意义。
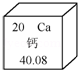
(1)在元素周期表中,钙元素的信息如图所示。钙元素的相对原子质量为。
(2)儿童缺钙可能会导致(填"贫血症"或"佝偻病")。
(3)氧化钙能与水反应,此反应可用于(填字母序号)。
| A. |
吸收水分 |
B. |
制熟石灰 |
C. |
加热食物 |
(4)熟石灰的化学式为,它可用于制备补碘剂
,其中碘元素的化学价为。
(5)"冰洲石"(主要成分为
)制成的工艺品不能与盐酸接触,用化学方程式表示其原因:。
目前常州市有两家垃圾焚烧发电厂,这两家焚烧厂处理了常州市绝大部分生活垃圾,每天一共处理垃圾2200吨。另外常州市还有一个垃圾填埋场,处于备用状态。
⑴ 垃圾焚烧发电技术不但解决了垃圾露天焚烧带来的环境污染问题,同时,可谓一举两得。
⑵ 垃圾焚烧发电的前提是分类收集生活垃圾,下列属于可燃垃圾的有。
| A.玻璃酒瓶 | B.旧报纸 | C.聚氯乙烯塑料 | D.碎瓷砖E.废弃棉质衣服 |
⑶ 垃圾焚烧时会产生一些有害气体如:二噁英(C12H4Cl4O2)、二氧化硫、氯化氢。二噁英中元素的质量分数最低;为了减少对环境的污染,发电厂通过喷熟石灰悬浊液反应处理这些气体,试写出其中一个反应的化学方程式。
不同温度下,碳酸钠和碳酸氢钠的溶解度如下表所示
| 温度/℃ |
0 |
20 |
40 |
60 |
| 碳酸钠 |
7.0 |
21.8 |
48.8 |
46.4 |
| 碳酸氢钠 |
6.9 |
9.6 |
12.7 |
16.4 |
(碳酸钠、碳酸氢钠)俗称小苏打(请在选择的物质下面划线)。
⑵ 服用碳酸氢钠治疗胃酸过多时,胃液的pH(填“增大”、“减小”或“不变”),发生反应的化学方程式是。
⑶ 为区分碳酸钠和碳酸氢钠两种白色固体。在20℃时,各盛有50 mL水的甲、乙两烧杯中,分别加入等质量的碳酸钠和碳酸氢钠固体,充分溶解后,现象如图所示。乙烧杯中加入的物质是(填化学式),加入的质量m的范围为:。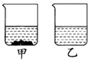
某化学兴趣小组在老师指导下制取、干燥、收集氨气,并探究氨气的一些性质。
资料卡片:氨气通常情况下是有刺激性气味的无色气体,密度比空气小,极易溶于水,易液化,液氨可作制冷剂。
加热熟石灰和氯化铵固体混合物的方法可以生成氨气。如要快速产生氨气,可以将浓氨水滴加到生石灰中得到。
⑴ 利用A装置制取氨气的化学方程式为。将浓氨水滴加到生石灰快速产生氨气,发生装置最好选用(选填装置编号)。请写出生石灰在此反应中的两个作用:,。
⑵ 干燥氨气可以将气体通过装有(填化学式)的装置D。
⑶ 兴趣小组计划用E装置收氨气,简述判断氨气已经集满的方法。
。
⑷ 按下图连接仪器后,计划在纯净水塑料瓶内引发喷泉,你会采取怎样的操作?。
⑸ 试验后为处理纯净水塑料瓶内存在的氨水(NH3•H2O)可以加入少量稀硫酸,发生反应的化学方程式为。
稀薄燃烧发动机具有高效、经济、环保等优点,和普通汽车发动机对比如下:
| 发动机类型 |
发动机混合气中汽 油与空气的质量比 |
发动机运 转时温度 |
尾气中 CO的含量 |
尾气中 NOx的含量 |
| 普通发动机 |
1:15 |
较高 |
较高 |
较高 |
| 稀薄燃烧发动机 |
1:40 |
较低 |
较低 |
较低 |
⑴ 根据上表的数据可知“稀薄”的含义是。
A.发动机混合气中的汽油含量低 B.发动机混合气中的空气含量低
C.发动机混合气中氧气的含量低 D.发动机混合气中氮气的含量低
⑵ 为何稀薄燃烧发动机产生的尾气中CO含量会减少?。
⑶ 某种减少尾气中CO与NOX的方法是使用催化转换器,转换过程中发生反应的化学方程式为:CO+NOx→CO2+N2(未配平)。若x = 1.5,则化学方程式中CO2与N2的系数之比为。
以化合价为纵坐标,以物质的类别为横坐标所绘制的图像叫价类图。下图为铁的价类图,请分析该图后填写: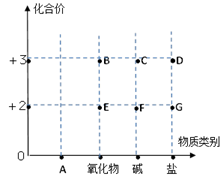
⑴ A点表示的物质类别是,
B点表示化合物的颜色为。
⑵ 某化合物化学式为(NH4)2Fe(SO4)2,它代表的点是(选填A、B、C、D、E、F、G)。
⑶ 写出由F点表示的化合物与氧气、水发生化合反应生成C的化学方程式。