以下是A、B、C、D、E、甲、乙几种物质相互转化的关系图: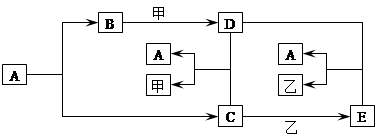
其中A是大理石的主要成分,甲是常用的重要溶剂,乙溶液中阳离子为Na+。
(1)写出下列物质的化学式:
A: ;B: ;甲: ;乙: 。
(2)写出D和E反应的化学方程式: 。
有A、B、C、D、E五种元素,A的单质是密度最小的气体;B的次外层电子数占电子总数的1/4;C的阳离子C+比B原子多2个电子;D和C具有相同的电子层数,D—的离子结构与氩原子结构相同;E和B具有相同的最外层电子数,但比B多一层。
(1)写出元素符号:A______、B______、C_______、D________、E________。
(2)画出D—的离子结构示意图:__________。
某元素R的结构示意图为: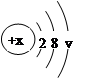 。
。
(1)当x=10+y时,该粒子为_______(填“原子”、“阳粒子”或“阴离子”),当x<10+y时,该粒子为__________。
(2)当y=2时x=_________。该元素能形成的离子符号为__________。
(3)若该结构示意图表示的粒子是R—,则x=__________,y=__________。
(11.分)有A、B、C、D、E五种常见物质,它们有如图所示的关系: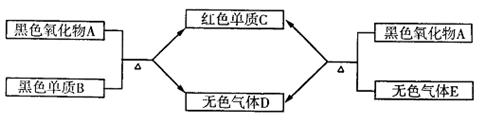
⑴已知:C是一种金属,气体D可以使澄清石灰水变浑浊,E气体有毒,能与人体内的血红蛋白结合,写出这五种物质的化学式:A.B.C.D.E.______
⑵写出图中A变成C的化学方程式;
。
(3)写出气体D使澄清石灰水变浑浊的化学方程式。
有A、B、C、D四种元素,A是地壳中含量最多的金属元素,B元素原子第三电子层比第二电子层少一个电子,C元素原子得到2个电子以及D元素原子失去一个电子后所得粒子均与氖原子具有相同的电子层结构,则:
(1)试写出下列元素符号:A;B;C;D;
(2)画出A的原子结构示意图:。
若A、B、C、D之间的关系如图所示。(图中“—”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,部分反应物、生成物及反应条件均已略去)A~D均含一种相同元素,且A、B、D均为氧化物,C是空气中的主要成分之一。则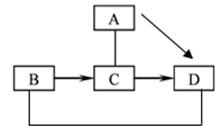
(1)C的化学式。
(2)实验室中制取物质D的反应方程式:。
(3)实现D转化A为的反应化学方程式是。