I.磷、硫元素的单质和化合物应用广泛。
(1)磷元素的原子结构示意图是 。
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500°C生成白磷,反应为:
2Ca3(PO4)2+6SiO2==6CaSiO3+P4O10 , 10C+P4O10==P4+10CO
每生成 1molP4时,就有 mol电子发生转移。
(3)硫代硫酸钠(Na2S2O3)是常用的还原剂。在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素C完全氧化,剩余的I2 用Na2S2O3溶液滴定,可测定溶液中维生素C的含量。发生的反应为:
C6H8O6+I2===C6H6O6+2H++2I- 2S2O32-+I2===S4O62-+2I-
在一定体积的某维生素C溶液中加入amolL-1I2溶液V1ml,充分反应后,用Na2S2O3溶液滴定剩余的I2,消耗bmolL-1 Na2S2O3溶液V2ml.该溶液中维生素C的物质量是 mol。
(4)在酸性溶液中,碘酸钠(KIO3)和亚硫酸钠可发生如下反映:
2IO3-+5SO32-+2H+==I2+5SO42++H2O
生成的碘可以用淀粉液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:
| |
0.01mol·L-1KIO3酸性溶液(含淀粉)的体积/mL |
0.01mol·L-1Na2SO3溶液的体积/mL |
H2O的体积/mL |
实验温度/℃ |
溶液出现蓝色时所需时间/s |
| 实验1 |
5 |
V1 |
35 |
25 |
|
| 实验2 |
5 |
5 |
40 |
25 |
|
| 实验3 |
5 |
5 |
V2 |
0 |
|
该实验的目的是______;表中V2=_________mL.
II稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位。
(5)在某强酸性混合稀土溶液中加入H2O2,调节pH ≈3. Ce3+通过下列反应形成Ce(OH)4沉淀得以分离。完成反应的离子方程式:
□Ce3++□H2O2+□H2O=====□Ce(OH)4↓+□
钠是一种很活泼的金属,在工业上常用电解熔融NaCl的方法制得,其另一产物氯气的用途也十分广泛,工业上制取漂白粉就是其用途之一。
(1)请写出工业上用电解方法制取钠的化学方程式。
(2)工业上制取漂白粉的化学反应方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉的主要成分是。
(3)实验室有一瓶密封不严的漂白粉,其中肯定存在CaCl2,请设计实验,探究该固体中可能存在的其它物质。①提出合理假设。
假设1:该漂白粉未变质,只含;
假设2:该漂白粉全部变质,只含;
假设3:该漂白粉部分变质,既含有Ca(ClO)2又含有CaCO3。
②设计实验方案,进行实验。请在答题卡上写出实验步骤、预期现象与结论
限选用的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、1mol/LHCl、品红溶液、新制澄清石灰水。(提示:不必检验Ca2+和Cl-,表格可以不填满。)
| 实验步骤 |
预期现象和结论 |
|
| ① |
取少量上述漂白粉于试管中, |
|
| ② |
||
| ③ |
磁材氧化铁的化学名称是氧化铁(Fe2O3),它是电子、电信工业的磁性材料,工业上采用生产钛白粉的下脚料(含大量FeSO4的废液)为原料来制备磁材氧化铁。

已知煅烧中的化学反应方程式为:FeCO3 → FeO + CO2↑,4FeO + O2 → 2Fe2O3
(1)用98%的H2SO4的配制500mL的20%的H2SO4,所需玻璃仪器是
| A.玻璃棒 | B.烧杯 | C.漏斗 | D.250mL容量瓶 |
E、500mL容量瓶 F、胶头滴管
(2)浓缩结晶后得到的晶体是(填化学式),A中溶质是;
此溶液中各离子的浓度比较大小为:。
(3)20%H2SO4和铁皮的作用分别是。
(4)检验滤液中含有NH4+的方法是
(5)写出步骤“合成”中发生的化学变化(用化学方程式表示):
。
现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题。(由实验装置引起的实验误差忽略不计)。
Ⅰ.探究浓硫酸的某些性质
(1)称量E的质量;按照图示连续装置,检查装置的气密性。
(2)将mg铁碳合金样品放入A中,再加入适量的浓硫酸。未点燃酒精灯前,A、B均无明显现象,其原因是:。点燃酒精灯一段时间后,B中可观察到的明显现象是。C中足量的酸性KMnO4溶液所起的作用是。D中盛放的试剂是。
(3)反应一段时间后,从A中逸出气体的速率仍然较快,除因反应温度较高外,还可能的原因是 。
。
Ⅱ.测定铁的质量分数
(4)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg,则铁碳合金中铁的质量分数为(写表达式)。某同学认为:依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,你认为可能的原因是。
(5)经过大家的讨论,决定采用上图装置和其他常用实验仪器测定某些数据即可,为了快速和准确地计算出铁的质量分数,最简便的实验操作是(填写代号)。
①用排水法测定H2的体积
②反应结束后,过滤、洗涤、干燥、称量残渣的质量
③测定反应前后装置和药品的总质量
喷泉是一种常见的现象,其产生的原因是存在压强差。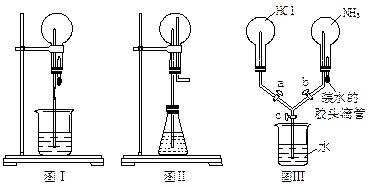
(1)图Ⅰ为化学教学中常用的喷泉实验装置。在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是
A. SO2和H2O B. CO2和NaOH溶液 C. NH3和H2O D. NO和H2O
(2)在图Ⅱ的锥形瓶中,分别加入足量的下列物质后,能产生喷泉的是
A. Cu与稀硫酸 B. Cu与稀硝酸 C. Al与浓硫酸 D. Fe与浓硝酸
(3)比较图Ⅰ和图Ⅱ两套装置,从产生喷泉的原理来分析,图Ⅰ是上部烧瓶内气体压强;图Ⅱ是下部锥形瓶内气体压强(填“增大”或“减小” )。
(4)某学生积极思考喷泉原理的应用,设计了如图Ⅲ所示的装置。
① 如果关闭活塞c,打开活塞a、b,再挤压胶头滴管。则可能出现的现象为。
② 在①操作的基础上,打开活塞c,产生的现象是。
某课外活动小组为探究CO2与过量的NaOH溶液确实发生了化学反应,甲、乙、丙三位同学设计了下列三种实验装置,请回答下列问题:
(1)甲装置中CO2与过量的NaOH反应的离子方程式。
(2)丙装置实验现象是,解释产生该实验现象的原因
。
(3)甲、乙、丙同学设计的三个方案中,有一个方案在实际操作中安全性存在问题,该方案是(填甲、乙或丙),原因是
。
(4)请设计一个实验检验生成的产物Na2CO3中的阴离子。(简述操作步骤、所用试剂、实验现象和结论。)
(5)实验室中若需用44.8 L(标准状态)CO2 ,现用含CaCO3 90%石灰石与足量的盐酸反应,至少需要这种石灰石 g