常温下,下列各组离子在溶液中一定能大量共存的是
| A.1.0mol/L的KNO3溶液:H+、Fe2+、Cl一、SO42一 |
| B.与铝反应产生大量氢气的溶液:Na+、K+、HCO3—、NO3一 |
C.pH=12的溶液: 、 、 、 、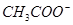 、Br- 、Br- |
D.由水电离产生的 的溶液: 的溶液: 、 、 、 、 、 、 |
将两种硫酸盐按一定比例混合后共熔,可制得化合物X,X溶于水能电离出K+、Cr3+、SO42-,若将2.83 g X中的Cr3+全部氧化为Cr2O72-后,溶液中的Cr2O72-可和过量KI溶液反应,得到3.81 g I2,反应的离子方程式为:Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,若向溶有2.83 g X的溶液中,加入过量的BaCl2溶液,可得到4.66 g白色沉淀。由此可推断出X的化学式为
| A.K2SO4·2Cr2(SO4)3 |
| B.2K2SO4·Cr2(SO4)3 |
| C.K2SO4·1/2Cr2(SO4)3 |
| D.K2SO4·Cr2(SO4)3 |
锑(Sb)在自然界一般以硫化物的形式存在,我国锑的蕴藏量为世界第一,从硫化物中提取单质锑一般是先在高温下将硫化物转化为氧化物,再用碳还原:
①2Sb2S3+3O2+6Fe Sb4O6+6FeS②Sb4O6+6C
Sb4O6+6FeS②Sb4O6+6C 4Sb+6CO↑,关于反应①、②的说法正确的是()
4Sb+6CO↑,关于反应①、②的说法正确的是()
A.反应①②中的氧化剂分别是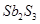 、 、 |
| B.反应②说明高温下C的还原性比Sb强 |
| C.反应①中每生成1mol FeS时,共转移3mol电子 |
| D.每生成4mol Sb时,反应①与反应②中还原剂的物质的量之比为4:3 |
阿伏加德罗常数的值为6.02×1023mol-1,下列叙述中错误的是:
①12.4g 白磷晶体中含有的P-P键数是0.6×6.02×1023
②含0.2mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0. 1×6.02×1023
③7.8g Na2S和Na2O2的混合物中含有的阴离子数大于0.1×6.02×1023
④2mol SO2和1mol O2在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数等于2×6.02×1023
⑤2.9g 2CaSO4•H2O含有的结晶水分子数为0.02×6.02×1023
| A.①②③④⑤ | B.①③④⑤ | C.②③④⑤ | D.③④⑤ |
下列各组物质相互混合反应后,最终有白色沉淀生成的是
①过量Na2O2投入到FeCl2溶液中②过量Ba(OH)2溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中④Na2SiO3溶液中通入过量CO2
⑤CaCl2与NaOH的混合溶液中通入过量CO2
| A.全部 | B.①⑤ | C.②③④ | D.②③④⑤ |