将经过酸洗除锈的铁钉,用饱和食盐水浸泡后放入如图所示的装置中,下列叙述正确是( )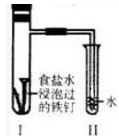
| A.过一段时间,Ⅱ试管中的导管内水柱上升 |
| B.Ⅰ试管中铁钉由于发生电解反应而被腐蚀 |
| C.铁钉在该试管中的腐蚀速度越来越快 |
| D.Ⅰ试管中铁钉发生反应的一个电极方程式为:2Cl—-2e—=Cl2↑ |
20℃时,将等质量的a、b两种固体,分别加入到盛有lO0g水的烧杯中,充分搅拌后现象如图甲,升温到50℃时,现象如图乙,a、b两种固体的溶解度曲线如图丙。下列说法正确的是
| A.图丙中M表示b的溶解度曲线 |
| B.图甲溶液中溶质的质量分数a大于b |
| C.图乙中a、b溶液一定是不饱和溶液 |
| D.30℃时a、b溶液溶质质量分数不相等 |
除去下列物质中的少量杂质,所选用试剂及操作方法均正确的是
| 选项 |
物质(括号内为杂质) |
选用试剂 |
操作方法 |
| A |
CO2(CO) |
过量O2 |
点燃 |
| B |
CaO(CaCO3) |
足量蒸馏水 |
过滤、蒸发 |
| C |
FeCl2溶液(CuCl2溶液) |
足量铁粉 |
过滤 |
| D |
NaCl溶液(MgSO4溶液) |
适量BaCl2溶液 |
过滤 |
如图所示为甲、乙两种固体的溶解度曲线,下列说法错误的是
| A.40℃时,甲的溶解度大于乙的溶解度 |
| B.20℃时,甲、乙两种物质的溶解度相等 |
| C.甲、乙两种物质的溶解度都随温度的升高而增大 |
| D.20℃时,把30g甲物质加入100g水中,充分溶解后所得溶液为饱和溶液 |
下列除去少量杂质的方法正确的是
| A.Zn粉中含少量的ZnO:加入足量稀H2SO4充分反应后过滤 |
| B.Cu(NO3)2溶液中含少量AgNO3:加入足量Cu屑充分反应后过滤 |
| C.Na2SO4溶液中含少量H2SO4:加入足量Ba(OH)2充分反应后过滤 |
| D.CaCO3固体中含少量Na2CO3:加入足量稀HCl充分反应后过滤 |
有关乙醇(C2H5OH)的说法正确的是
A.乙醇是食醋的主要成分
B.C2H5OH中C、H、O元素的质量比是2:6:1
C.乙醇不能溶于水
D.C2H5OH中C元素的质量分数是52%