向100克盐酸和氯化钙溶液的混物中逐滴滴入10.6%碳酸钠溶掖,且参加反应的碳酸钠溶液的质量与生成沉淀的质量之间的关系如图所示,
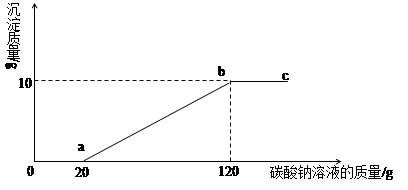
(1) a点溶液中的溶质是____________,b点溶液中的溶质是___________
(2)试计算到a点时所产生气体的总质量和b点时溶液的总质量(保留两位小数)
地沟油中含有一种强烈致癌物黄曲霉素B2(C17H14O6),长期食用会引起消化道癌变,请回答:
(1)黄曲霉素B2的相对分子质量为;
(2)黄曲霉素B2中碳、氢、氧三种元素的原子个数比为;
(3)15.7 g黄曲霉素B2中含有g氧元素。
在通入空气并加热的条件下,铜与稀硫酸反应转化为硫酸铜。
(1)请完成该反应的化学方程式:
2Cu+2H2SO4+O2 2CuSO4+
2CuSO4+
(2)利用此反应,将含铜80%的废料与10%的稀硫酸反应转化为10%的硫酸铜溶液,计算要得到1600g10%的硫酸铜溶液,需要加入稀硫酸的质量和水的质量(假设杂质不参加反应,也不溶于水)。
过氧化氢溶液长期保存会自然分解,使得溶质质量分数减小.小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定溶质质量分数.他们取出该溶液51g,加入适量二氧化锰,生成气体的质量与反应时间的关系如图所示.
(1)加入二氧化锰的作用是。
(2)完全反应后生成氧气的质量为 .
(3)计算该溶液中溶质的质量分数.
在电缆生产过程中会产生一定量的含铜废料。据报道,在通入空气并加热的条件下,铜与稀硫酸反应转化为硫酸铜。反应的化学方程式:2Cu + 2H2SO4 + O2 2CuSO4 + 2H2O取一定量溶质的质量分数为10%的稀硫酸(其中含溶质49 g),与铜恰好完全反应,假设其他杂质不反应也不溶解,则反应后硫酸铜溶液中溶质的质量分数是多少?
2CuSO4 + 2H2O取一定量溶质的质量分数为10%的稀硫酸(其中含溶质49 g),与铜恰好完全反应,假设其他杂质不反应也不溶解,则反应后硫酸铜溶液中溶质的质量分数是多少?
叠氮化钠(NaN3)受撞击时能在瞬间完全分解为钠和氮气,故可应用于汽车安全气囊。若产生56克(标准状况下体积为44.8升)的氮气,应在气囊内填充叠氮化钠(NaN3)的质量是多少?