实验室里常用锌和稀硫酸反应来制取氢气。林辉同学取6.5g的锌并加入50g一定质量分数的硫酸溶液,恰好完全反应后,得到56.3g硫酸锌溶液。发生反应的化学方程式是:Zn+H2SO4=ZnSO4+H2↑。请你计算:
(1)生成氢气的质量为_____________g。
(2)硫酸溶液中溶质的质量分数。
普通黄铜由铜和锌组成,广泛用于制造板材、管材等,也用于铸造机械零件等。为了测定某黄铜样品中铜的含量,设计了如下实验方案。取50.00g黄铜样品,加入一种未知浓度的稀盐酸。有关实验数据如下图。
(1)样品完全反应产生H2的质量___________。
(2)图中m与n的关系是mn(填“>”、“<”或“﹦”)。
(3)黄铜样品中铜的质量分数是多少(写出计算过程,保留小数点后一位)。
(4)某同学根据图中数据计算盐酸的溶质质量分数为: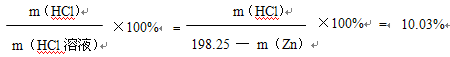
请分析该同学的计算结果是否正确,如不正确指出错误的原因:。
某化工厂用氢氧化钠溶液来吸收废气中的二氧化硫,有效地防止了酸雨的形成(假定废气中只有二氧硫能与氢氧化钠溶液反应、且二氧化硫与氢氧化钠溶液反应完全。反应的化学方程式为:SO2+2NaOH=Na2SO3+H2O)。该化工厂每天消耗8t质量分数为10%的氢氧化钠溶液。
(1)8t质量分数为10%的氢氧化钠溶液中含氢氧化钠_________t。
(2)求:该化工厂每天吸收的二氧化硫的质量。
无土栽培黄瓜的营养液的配方中,含有质量分数为0.2%的尿素溶液 [尿素的化学式为CO(NH2)2 ]。请通过计算,回答下列问题:
(1)尿素的相对分子质量为__________________。
(2)尿素中氮元素的质量分数为______________(精确到0.1%)。
(3)若用50 kg溶质的质量分数为2%的尿素溶液加水稀释,可得溶质的质量分数为0.2%的尿素溶液________kg。
黄铜是铜、锌合金,它可用来制造机器、电器零件及日用品。某化学兴趣小组取含铜35%的黄铜样品20克,加入到100g稀硫酸中。(假设样品中不含其它杂质)
①该黄铜样品中含铜的质量是_______,
②若稀硫酸恰好完全反应,则该稀硫酸中溶质的质量分数是多少?(反应方程式:Zn + H2SO4 = ZnSO4 + H2 )
某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用2.0 g石灰石样品,把25.0g质量分数为10%的稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如下:
| 实验次数 |
1 |
2 |
3 |
4 |
5 |
| 稀盐酸的累计加入量 |
5.0g |
10.0g |
15.0g |
20.0g |
25.0 g |
| 剩余固体的质量 |
1.5g |
1.0g |
0.5g |
0.3g |
0.3g |
请计算:
(1)2.0g石灰石样品中碳酸钙的质量为,石灰石中碳酸钙的质量分数为。
(2)请你继续计算反应生成溶液中氯化钙的质量分数(计算过程和结果均保留一位小数)。