向FeI2和FeBr2物质的量之比为2:3的混合溶液中逐滴滴入氯水,下列离子反应可能发生的是
| A.10Fe2+ + 8I-+4Br-+11Cl2 →10Fe3+ +4I2+2Br2+22Cl- |
| B.2Fe2+ +2I-+2Cl2 →2Fe3+ +I2+4Cl- |
| C.6Fe2+ +4I-+5Cl2 →6Fe3+ +2I2+10Cl- |
| D.6Fe2+ + 2I-+6Br-+7Cl2 →6Fe3+ +I2+3Br2+14Cl- |
有下列物质:① NaOH固体;② 浓硫酸;③ NH4NO3晶体;④ CaO固体。现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如右图所示状态,判断加入的物质可能是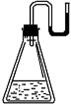
| A.① ② ③ ④ | B.① ② ④ |
| C.② ③ ④ | D.① ② ③ |
各组性质比较的表示中,正确的是 ( )。
| A.酸性:HI < HBr < HCl < HF | B.稳定性:HF< HCl < HBr < HI |
| C.氧化性:F2 < Cl2 < Br2 < I2 | D.沸点:F2 < Cl2 < Br2 < I2 |
已知反应X+Y=M+N为吸热反应,对这个反应的下列说法中正确的是
| A.X的能量一定低于M的能量,Y的能量一定低于N的能量 |
| B.因为该反应为吸热反应,故一定要加热反应才能进行 |
| C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 |
| D.X和Y的总能量一定低于M和N的总能量 |
X、Y、Z为同周期的三种元素。已知它们最高价氧化物的水化物的酸性由强到弱顺序为HXO4>H2YO4>H3ZO4,则下列判断正确的是
| A.非金属性X<Y<Z | B.原子半径X>Y>Z |
| C.气态氢化物的稳定性X>Y>Z | D.原子最外层电子数X<Y<Z |
下列各组元素性质的递变情况中,错误的是
A.Li、Be、B原子的最高正价依次增大
B.P、S、Cl元素的最高价氧化物对应水化物的酸性依次增强
C.B、C、N、O、F的原子半径依次增大
D.Li、Na、K、Rb元素的金属性依次增强