一定量的氢气在氯气中燃烧,所得混合物冷却后用500mL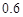 mol·L
mol·L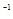 的NaOH溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为
的NaOH溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为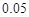 mol,参加反应的氢气和所用氯气的物质的量之比为( )
mol,参加反应的氢气和所用氯气的物质的量之比为( )
A.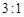 |
B.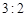 |
C. |
D.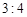 |
下列热化学方程式中,ΔH能正确表示物质的燃烧热的是
| A.CO(g)+1/2O2(g)====CO2(g) ΔH=-283.0 kJ·mol-1 |
| B.C(s)+1/2O2(g)====CO(g) ΔH=-110.5 kJ·mol-1 |
| C.H2(g)+1/2O2(g)====H2O(g) ΔH=-241.8 kJ·mol-1 |
| D.2C8H18(l)+25O2(g)====16CO2(g)+18 H2O(l) ΔH=-11 036 kJ·mol-1 |
下列叙述正确的是
| A.推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应 |
| B.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” |
| C.用电解水的方法制取大量氢气可以缓解能源不足的问题 |
| D.由于我国煤和石油的储量十分丰富,所以太阳能和核能的开发在我国并不十分重要 |
在一个密闭容器中发生如下反应:2SO2 (g)+O2(g) 2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达到平衡时,可能出现的数据是
2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达到平衡时,可能出现的数据是
| A.c(SO3)=0.4 mol·L-1 | B.c(SO3)+c(SO2)=0.15 mol·L-1 |
| C.c(O2)=0.3 mol·L-1 | D.c(SO3)+c(SO2)=0.4 mol·L-1 |
一定温度下,向容积为2 L的密闭容器通入两种气体发生化学反应,反应中各物质的物质的量变化如右图所示,对该反应的推断合理的是
A.该反应的化学方程式为3B+4D====6A+2C
B.反应进行到1 s时,v(A)=v(D)
C.反应进行到6 s时,B的平均反应速率为0.05 mol·(L·s) -1
D.反应进行到6 s时,各物质的反应速率相等
反应CO+H2O(g) CO2+H2在1 000 K达到平衡时,分别改变下列条件,K值发生变化的是
CO2+H2在1 000 K达到平衡时,分别改变下列条件,K值发生变化的是
| A.将压强减小至原来的一半 | B.将反应温度升高至1 200 K |
| C.添加催化剂 | D.增大水蒸气的浓度 |