关于原子轨道的说法正确的是
| A.凡是中心原子采取sp3杂化轨道成键的分子其立体构型都是正四面体形 |
| B.CH4分子中sp3杂化轨道是4个H原子的1s轨道和C原子的2p轨道混合起来而形成的 |
| C.sp3杂化轨道是由同一个原子中能量相近的s轨道和p轨道混合形成的一组能量相近的新轨道 |
| D.凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键 |
下列有关说法正确的是()
| A.焓变就是反应热,化学变化中存在焓变,物理变化中不存在焓变。 |
| B.电解池中与直流电源正极相连的是阳极,阳极发生氧化反应;与电源负极相连的是阴极,阴极发生还原反应。通电时,电子的流向为负极→阴极→电解质→阳极→正极 |
| C.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1 |
| D.CO(g)的燃烧热是ΔH=-283.0 kJ·mol-1,则反应CO2(g)===CO(g)+1/2O2(g)的反应热ΔH=+283.0 kJ·mol-1 |
化学与能源、生产、生活密切相关。下列说法正确的是()
| A.气象环境报告中的“PM2.5”是对一种新分子的描述 |
| B.高铁车厢采用的铝合金材料强度大、质量轻,不与氧气反应 |
| C.煤经气化和液化两个物理变化过程,可变为清洁能源 |
| D.利用太阳能等新能源代替化石燃料,有利于改善大气质量、保护环境 |
将11.2g的Mg—Cu混合物完全溶解于足量的硝酸中,收集反应产生的x气体。再向所得溶液中加入适量的NaOH溶液,产生21.4g沉淀。根据题意推断气体x的成分可能是
| A.0.3mol NO2和0.3mol NO |
| B.0.2mol NO2和0.2mol N2O4 |
| C.0.1mol NO、0.2mol NO2和0.05mol N2O4 |
| D.0.6mol NO |
T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图-1所示;若保持其他条件不变,温度分别为T1和T2,Y的体积百分含量与时间的关系如图-2所示。下列分析正确的是
A.容器中发生的反应可表示为:3X(g)+Y(g) 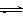 2Z(g) 2Z(g) |
| B.0~3 min内,v(X)=0.2 mol•L-1•min-1 |
| C.其他条件不变升高温度,v正、v逆都增大,且重新平衡前v正>v逆 |
| D.若改变条件,使反应进程如图-3所示,则改变的条件可能是增大压强 |
在溶液中加入少量Na2O2后仍能大量共存的离子组是
| A.NH4+、Ba2+、Cl-、NO3- | B.K+、AlO2-、Cl-、SO42- |
| C.Ca2+、Mg2+、NO3-、HCO3- | D.Na+、Cl-、CO32-、SO32- |