实验室有一瓶久置的氢氧化钠固体,某同学想了解其变质的情况,设计了以下实验:
实验一:取少量样品于试管中,滴加适量稀盐酸,观察到有气泡产生,说明氢氧化钠已变质,变质的原因是 (用化学方程式表示)
实验二: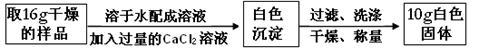
通过实验二,能进一步推算出氢氧化钠变质的程度。
(1)求16 g该样品中碳酸钠的质量分数。
(2)通过实验一的分析和(1)的计算结果,可计算出样品中已经变质的氢氧化钠,则16g干燥的样品中已变质的氢氧化钠的质量是 g。
将 氯化钙溶液和 碳酸钠溶液混合后,恰好完全反应.过滤后得到 溶液.请计算:
(1)反应后生成沉淀的质量.
(2)过滤后所得溶液中溶质的质量分数.
高温加热10g碳酸钙,一段时间后停止加热,测得剩余固体中钙元素的质量分数为50%。
(1)若10g碳酸钙全部分解可产生多少克氧化钙?
(2)实际反应生成的二氧化碳是多少克?
如图为A、B两种固体物质的溶解度曲线。
(1)在℃时,A、B两种物质的溶解度相等。
(2)t2℃时,100g水中溶解gA物质恰好饱和,该饱和溶液中溶质的质量分数为。若要把该饱和溶液稀释成质量分数为1 0%的溶液,应加水g。
(3)t2℃时,分别将恰好饱和的A、B两种物质的溶液降温至t1℃,溶质的质量分数保持不变的是。
某地一辆满载浓硫酸的罐车翻到,导致25
溶质的质量分数为98%的浓硫酸泄漏,并向路基两边蔓延,接到报警后消防官兵立即赶来并用石灰浆(主要成分为氢氧化钙)中和硫酸解除了险情。请回答:
(1)25
溶质的质量分数为98%的浓硫酸中含
的质量为;
(2)计算:中和泄漏的硫酸,理论上需要多少吨氢氧化钙;
(3)处理一定量的硫酸,理论上既可用
吨的氢氧化钙粉末,也可选用
吨的氧化钙粉末,还可用
吨碳酸钙粉末,则
、
、
的数值大小关系为。
医学上常用双氧水来清洗创口和局部抗菌。小美同学为了测定一瓶医用双氧水溶液的溶质质量分数,取该双氧水69
放入烧杯中,然后加入2
二氧化锰,完全反应后,称得烧杯内剩余物质的总质量为69.04
。请回答下列问题;
(1)二氧化锰在反应中的作用是,生成的氧气为
。
(2)该双氧水溶液的溶质质量分数。(写出计算过程)