“保护环境,就是保护自己。”下列各组中的四种物质都是大气污染物的是( )
| A.SO2、NO2、CO、烟尘 | B.CO2、Cl2、N2、雾 |
| C.HCl、NO2、N2、粉尘 | D.O2、NO、NH3、H2S |
已知气体的摩 尔质量越小,扩散速度越快。右图所示为气体扩散速度的试验,两种气体扩散相遇时形成白色烟环。下列关于物质甲、乙的
尔质量越小,扩散速度越快。右图所示为气体扩散速度的试验,两种气体扩散相遇时形成白色烟环。下列关于物质甲、乙的 判断正确的是
判断正确的是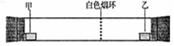
| A.甲是浓氨水,乙是浓硫酸 | B.甲是浓盐酸,乙是浓氨水 |
| C.甲是浓氨水,乙是浓盐酸 | D.甲是浓硝酸 ,乙是浓氨水 ,乙是浓氨水 |
已知:
① CH4 ( g )+4NO2( g )="4NO(" g ) +CO2( g )+2H2O( g ) △H=一574 kJ·mol-1
② CH4 ( g )+4NO( g )=2N2( g )+CO2( g )+2H2O( g ) △H=一1 160 kJ·mol一1。
下列正确的选项是
| A.CH4 ( g )+2NO2 ( g )= N2( g )+CO2 ( g )+2H2O ( l) △H=一867 kJ·mol-1 |
| B.CH4 ( g )+2NO2 ( g )= N2( g )+CO2 ( g )+2H2O ( g) △H=一867 kJ·mol-1 |
| C.CH4 ( g )+2NO2 ( g )= N2( g )+CO2 ( g )+2H2O ( g) △H=一586kJ·mol-1 |
| D.CH4 ( g )+2NO2 ( g )= N2( g )+CO2 ( g )+2H2O ( g) △H=+586kJ·mol-1 |
将0.l mol∙L-1的下列物质的水溶液,从常温加热到80℃,溶液的pH不变的是
| A.NaCl | B.NaOH | C.H2SO4 | D.NH4Cl |
分别在PH=1的酸溶液和PH=14的NaOH溶液中加入足量的铝,放出氢气的量前者多,其原因可能是:①两溶液的体积相同,而酸是多元强酸;②两溶液的体积相同,酸是弱酸;③酸溶液的体积比NaOH溶液体积大;④酸是强酸,且酸溶液的浓度比NaOH溶液浓度大;其中正确的为
| A.只有②和③ | B.只有②和④ | C.只有①和③ | D.只有① |
用标准盐酸滴定未知浓度的NaOH溶液时,下列操作能引起偏低误差的是
| A.锥形瓶用待测液润洗2~3次 |
| B.指示剂变色后又立即就停止滴定 |
| C.滴定前酸式滴定管俯视读数,滴定后又仰视 |
| D.滴定结束后,酸式滴定管尖嘴处悬挂一滴液体 |