用标准盐酸滴定未知浓度的NaOH溶液时,若测定结果偏高,则产生误差的原因可能是( )
| A.滴定时,装NaOH溶液的锥形瓶未用NaOH溶液润洗 |
| B.酸式滴定管用蒸馏水洗后,用标准盐酸润洗 |
| C.滴定前,酸式滴定管尖嘴处有气泡,而在滴定后气泡消失 |
| D.配制NaOH溶液时,NaOH固体中混有少量KOH固体 |
下列化合物中,既有离子键,又有共价键的是 ( )
| A.H2O | B.CaCl2 | C.KOH | D.NH3 |
卤族元素随着原子序数的增大,下列递变规律正确的是 ( )
| A.单质熔、沸点逐渐降低 | B.单质的氧化性逐渐增强 |
| C.原子半径逐渐增大 | D.气态氢化物稳定性逐渐增强 |
在一定条件下,对于密闭容器中进行的可逆反应A(g)+3B(g) 2C(g),下列说法中,能说明这一反应已经达到化学平衡状态的是( )
2C(g),下列说法中,能说明这一反应已经达到化学平衡状态的是( )
A.生成C的速率与C分解的速率相等
B.A、B、C的浓度相等
C.单位时间生成 n mol A,同时生成 3n mol B
D.A、B、C的分子数之比为 1∶3∶2
汽车尾气中的有毒气体NO和CO,在一定条件下可发生反应生成N2和CO2。下列关于此反应的说法中,正确的是 ( )
| A.减小压强能增大反应速率 | B.增大压强能减小反应速率 |
| C.使用适当的催化剂能增大反应速率 | D.升高温度对反应速率无影响 |
下列各组物质中,互称为同分异构体的是 ( )
| A.水与冰 | B.O2与O3 |
C. |
D.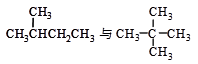 |